
Светлое и темное
Все существа носят в себе инь и ян, наполнены ци и образуют гармонию.
Свет и тьма, их непреложность, чередование, бесконечный, но неутомительный хоровод - так уж устроена жизнь, и неудивительно, что и растениям необходимо и то и другое. Простая мысль, Однако лишь в самом начале нашего века физиологи растений начали осознавать это, а решающие доказательства и вовсе были получены лишь в последние десятилетия...
1
И Волга начинается с ручейка.
Ф. Блэкман, физиолог растений, англичанин. Видимо, это был скромный исследователь, и чем дальше, тем менее его вспоминают. Но в 1905 году он положил начало целому громадному этапу новейших исследований фотосинтеза.
(В том же 1905 году Эйнштейн опубликовал специальную теорию относительности. Она потрясла умы. Открытие Блэкмана оценил лишь очень узкий круг специалистов: час Биологии еще не пробил!
Тут же заметим: мы способны проследить каждый шаг Ньютона - кто не слышал, к примеру, про знаменитое яблоко, якобы стукнувшее его по голове? Но нам - имеется в виду "широкий читатель" - ничего не говорят или очень мало имена Пристли, Ва.рбурга, даже нашего выдающегося соотечественника Алексея Николаевича Баха, революционера и ученого, основателя школы советских биохимиков, человека, который еще в 1893 году лучше чем кто-нибудь другой в мире понимал суть фотосинтеза...)
Но вернемся к Блэкману. К тому времени о фотосинтезе было известно немногое - только то, что и углекислый газ, и свет, и вода, исчезая в листе, как-то образуют в нем кислород да глюкозу (крахмал, его гигантские молекулы массой в 50 тысяч, получается из крошечных молекул глюкозы путем полимеризации - однотипного наращивания, как снежный ком из снежинок).
Выражаясь языком кибернетиков, фотосинтез был для исследователей "черным ящиком": эти магические для непосвященных слова означают просто полное отсутствие знаний о внутреннем устройстве того или иного объекта.
Блэкман, естественно, не был знаком с кибернетикой, но он понимал, что у него в руках две "веревочки" (углекислота и свет), дергая за которые он, видимо, кое-что сможет узнать про фотосинтез.
Это и есть соль его работы.
Попробуем изменять интенсивность освещения листа. Когда свет очень слабый, продуктивность фотосинтеза, о которой судят по количеству образовавшегося крахмала, целиком зависит от освещения и растет вместе с ним. Но лишь до некоторого предела.
Рано или поздно наступает момент, когда фактор освещения перестает действовать (кабы не это, любой урожай был бы в наших руках; все упиралось бы в энергию: делай свет все ярче и ярче и получишь столько зерен, зелени, хлопка, сколько захочешь!).
Как объяснить этот экспериментальный факт? В листе процесс фотосинтеза распадается на две по крайней мере стадии: есть реакции световые, целиком определяемые качеством и количеством света, и темновые, от света не зависящие, идущие даже в темноте.
Вот аналогия, которая нам поможет. Допустим, необходимо в курортный сезон переправить из Москвы на Кавказ как можно больше людей. К аэропортам мчат тысячи автобусов-экспрессов: они везут и везут пассажиров. Однако в аэропорту давка, гвалт, толкотня, неразбериха и паника, ибо самолеты не могут поднять в воздух всех желающих: да просто не хватает лайнеров!..
Так же и в фотосинтезе: яркий свет несет миллионы фотонов, но в растении есть какие-то идущие в темноте, темновые (их прежде называли "блэкмановскими") реакции, стадии, на которые свет (число автомашин в нашей аналогии) уже никак не может повлиять. И процесс выходит на насыщение.
Легко вообразить, что результаты были бы такими же, если бы мы варьировали не силу света, а концентрацию в воздухе углекислого газа...
2
Через 27 лет после публикации работы Блэкмана был сделан еще один очень важный шаг.
Что лучше? Яркое солнце над головой, щедро и без устали изливающее свои лучи, или же такая (фантастическая для землян) картина: ночная мгла, которая через каждые несколько секунд прерывается короткими солнечными вспышками?
Солнце-прожектор или солнце-маяк?
Странные, казалось бы, вопросы, но именно их, по сути, и поставили в 1932 году два американских биохимика - Р. Эмерсон и В. Арнольд.
Исследователи освещали растительные клетки короткими вспышками света, импульсами, за которыми следовали периоды темноты.
Выяснилось, что темновая стадия должна быть во много раз длительнее световой. Этого требовали сами растения - показателем была их продуктивность.
Так светлая и темная стороны жизни растений проявили себя совершенно отчетливо и недвусмысленно.
Эмерсон и Арнольд следующим образом истолковали свои данные: во время световой вспышки растение запасаег энергию, она необходима для успешного хода каких-то темповых процессов, видимо связанных с фиксацией в растении углекислого газа. Процесс фиксации углекислого газа в отличие от светового идет медленно, и пока он не завершится, бесполезно вводить в растение новые порции световой энергии.
Эти давние сугубо вроде бы научные изыскания имели в наши дни неожиданное продолжение.
Растения - наши кормильцы: они ублажают нас всевозможными яствами. Да, они довольно капризны: хорошо плодоносят не в любых условиях, требуют внимания и забот. И тут, если мы заинтересованы в урожае, необходимо уважить любую их прихоть.
И, если им так уж необходимо солнце-маяк, что ж, надо пойти им навстречу - так решили биологи, работающие в Ленинградском сельскохозяйственном институте.
Мигающее солнце? Нате!
В институте была сооружела специальная теплица. В ней длящиеся мгновения "дни" сменяли долгие (несколько секунд) "ночи".
Словно огни маяка, все искусственные светила теплицы по команде расторопной автоматики дружно мигали, создавая необычные даже для космонавтов условия жизни.
Но то, что не понравилось бы космонавтам, пришлось явно по вкусу зеленым питомцам, разместившимся на грядках этого фантастического мирка.
Опыт ленинградцев повторили овощеводы Мурманска, Гомеля и других городов. И не пожалели об этом: урожаи значительно возросли, а вот расход электроэнергии резко сократился. А ведь при выращивании в теплицах огурцов и помидоров львиную долю расходов составляет именно оплата электроэнергии!
(При умелом регулировании света, утверждают ленинградские ученые, нужды на электроэнергию в теплицах можно сократить в 400 раз!)
Светлое и темное - здесь много загадок, исследователям еще придется поломать над ними голову.
Ну вот хотя бы понятие "урожайный год". Что это такое: только ли обилие влаги, тепла, "африканского" солнца? Конечно, нет.
Оказывается, у растений бывают дни, когда они растут, словно на дрожжах. И это случается, как выяснили те же ленинградцы, если по небу чередой бегут облака, то закрывая, то приоткрывая солнышко...
Так возник еще один вариант, сулящий растениям в теплицах небывалый комфорт. Теперь под стеклянной крышей ученые держали постоянный невысокий световой фон (имитация пасмурных дней). Но время от времени давали еще и сильные светозые удары-вспышки (солнце из-за туч). И эта пропись физиологов растений оказалась для зелени также поистине чудотворной!..
3
Байер (1835-1917), немецкий химик-органик, сын прусского генерала, который интересовался науками и даже стал главой Берлинского геодезического института. Байер - сын учился в Гейдельберге у Бунзена и Кекуле, в 1875 году уже известным ученым он переехал в Мюнхен и занял там место умершего Либиха. Здесь Байер создал громадную школу (из нее вышли многие выдающиеся немецкие химики), завершил за 60 лет работы около 300 научных исследований. В 1863 году он открыл "сонные пилюли" барбитураты (есть версия, что пилюли названы так в честь одной знакомой Байера - Барбары), в 1878-1883 годы установил структуру и синтезировал один из важнейших природных красителей - индиго. Эти работы в 1905 году были увенчаны Нобелевской премией.
То, что фотосинтез делится на стадии - темновую и световую, было ценным открытием. Но что же все-таки происходит там, внутри, в недрах растительной клетки? Какие именно химические процессы? Что, собственно, катализирует хлорофилл?..
Еще одна возможность заглянуть в "черный ящик" - это попытаться выяснить: что служит в растении источником кислорода - вода или углекислый газ? Ведь и то, и другое соединение включает в себя кислородные атомы.
(Иногда бывает полезно заняться умственными спекуляциями, манипулированием исходными и конечными данными, всевозможным их комбинированием.
Так в наше время довольно часто, и порой весьма успешно, действуют физики-теоретики. Вооружившись соображениями симметрии, законами сохранения и новейшей математикой - теорией групп, американец М. Гелл-Ман в 1963 году стал раскладывать всевозможные пасьянсы из накопившегося к тому времени великого множества элементарных частиц. В конце концов он пришел к идее кварков - трех необычных частиц с дробными зарядами: до этих пор заряды всегда оказывались кратными целому числу. Кварки - название было заимствовано из фантастического романа ирландского писателя Джойса - вначале были встречены в штыки. Однако теория кварков предсказывала существование новой частицы, которая вскоре и была обнаружена. Успех был полный. В 1969 году Гелл-Ман стал Нобелевским лауреатом.)
Кажется довольно естественным, чтобы молекула кислорода (02) в растении выделялась из углекислого газа (С02), а углерод (С), присоединяя воду (Н20), образовывал углеводы - комбинации атомов типа С(Н20)-отсюда и название "углеводы".
Так, например, химическая формула глюкозы - одного из первичных продуктов фотосинтеза - С6Н12О6, ее можно написать также - (С(Н20))6.
Значительно труднее обосновать предположение о том, что растения выделяют кислород из воды, хотя бы потому, что в воде атомарный кислород (О) придется объединять в молекулу (О2).
В 1870 году Иоганн Фридрих Вильгельм Адольф Байер, глава немецких химиков-органиков, выдвинул гипотезу о формальдегиде; и она прочно утвердилась в ботанической литературе.
Формальдегид - простейший из углеводов: СН2О - вот его формула.
Это, утверждал Байер, и есть тот кирпичик, из которого в растении и складывается все остальное. Шесть молекул формальдегида (нетрудно убедиться) должны дать одну молекулу глюкозы.
И действительно, при полимеризации формальдегида в колбе могут образовываться сахароподобные вещества. Это в 1861 году впервые продемонстрировал выдающийся русский химик Александр Михайлович Бутлеров.
Так-то оно так, но одно дело стеклянная колба, другое - живой лист!..
Начались поиски: в растительных клетках искали формальдегид. На это дело ушли многие десятки лет, уйма ученых трудов, учено-дней, если говорить языком бухгалтеров и статистиков.
Обнаружили: формальдегид крайне ядовит для растений. Но, возражали сторонники Байера, в клетке формальдегид превращается в глюкозу чрезвычайно быстро, и он присутствует там в ничтожных дбзах...
Превращение в химической лаборатории формальдегида в сахар - очень нудная, длительная и утомительная процедура. И на это нашелся ответ:. то, что трудно нам, людям, с тем шутя справляются растения. Их чудесные ферменты сокращают долгие часы до мгновений, говорили приверженцы формальдегидной теории...
Гипотеза Байера была проста, изящна, а потому казалась верной. Ее изложение на протяжении почти трех четвертей столетия можно было найти в любом учебнике. Только очень мощный толчок мог поколебать и опрокинуть этот устоявшийся взгляд. Необходимо было на старую биологическую проблему взглянуть свежими глазами другой науки.
И это сделала физика.
4
Содди (1877-1956), английский радиохимик, окончил Оксфордский университет в Англии, затем работал под руководством Резерфорда в Канаде; вернувшись в 1904 году на родину, сотрудничал с Рамзаем. Предложил (совместно с Резерфордом) теорию радиоактивного распада, в 1913 году ввел понятие изотопов, за это открытие, сыгравшее огромную роль в развитии учения об атоме и атомном ядре, Содди в 1921 году получил Нобелевскую премию по химии. Рано (1936) отошел от науки и от преподавательской деятельности (причины: смерть жены, которую он тяжело переживал, и крайняя резкость суждений, которые он не находил нужным скрывать от окружающих). В честь Содди назван минерал соддит (силикат урана). Был иностранным членом-короеспондентом Академии наук СССР (1924).
Классификация Менделеева торжествовала одну победу за другой. Пустые прежде клеточки его таблицы успешно заполнялись, и вскоре свободных мест осталось совсем мало.
Тридцать лет периодический закон Менделеева успешно выдерживал все испытания и нападки. Но решающий экзамен еще только предстоял.
В 1896 году французский физик Антуан Анри Беккерель (самый знаменитый из четырех Беккерелей-физиков) обнаружил, что уран испускает неизвестного вида проникающее излучение.
Позже выяснилось: при распаде уран разваливается на радиоактивные куски, которые также могут дробиться, те в свою очередь распадаются... Вскоре подобное же свойство обнаружилось у тория.
Химики изучили до 40 таких атомов-осколков. Каждый имел собственные химические свойства, но - увы! - в периодической таблице Менделеева для новичков просто не было свободных мест. Как быть?
Эту проблему в 1913 году разрешил Фредерик Содди. Он предположил, что один и тот же элемент может обладать атомами различных типов.
Содди предложил вещества, идентичные по химическим свойствам, но различающиеся по массе и некоторым другим характеристикам, помещать (все семейство, сколь бы многочисленным оно ни было) в одну и ту же клетку периодической таблицы. И дал им название - изотопы ("равноместные" по-гречески).
Главное различие между изотопами - их масса. Ее обычно указывают справа вверху над химическим символом элемента.
Исключение сделали лишь для водорода: все три его изотопа имеют собственные имена и символы: протий (символ Н, это основная модификация), дейтерий (D) и тритий (Т).
Все они содержат по электрону и положительно заряженному протону, а потому и обладают одинаковыми химическими свойствами и должны быть помещены в одном и том же (первом) месте таблицы Менделеева.
Но вот масса их различна. В дейтерии к протону и электрону добавлен нейтрон, и масса дейтерия увеличилась против массы протия вдвое (крошечная масса электрона не в счет, а массы протона и нейтрона примерно одинаковы). Тритий тяжелее протия уже на две массы нейтрона.
Открытие в 1932 году дейтерия вызвало бурную дискуссию ученых: изотоп ли дейтерий или новый элемент?
А дело было в том, что, если в обычной, с протием, воде (Н20) заменить протий дейтерием, получим так называемую тяжелую воду - D20, обладающую удивительными свойствами: растения в ней развиваются с трудом, а живность - рыбы, лягушки, крабы - и вовсе быстро гибнет.
(Возникло даже предположение - сейчас оно опровергнуто, - что старость - это следствие постепенного накопления в организме человека тяжелой воды, тормозящей жизненные процессы...)
Дейтерий и тритий все же не делают погоды, их в природе крайне мало: так, во всем Черном море содержится всего 0,1 грамма трития.
А необычные свойства тяжелой воды объясняются так: в ней химические связи несколько прочнее, чем в воде обычной...
Мы привыкли к слову "изотопы", а ведь некогда их появление все перевернуло..
Прежде считалось, что все атомы данного вещества (этакие круглые шарики) ну абсолютно одинаковы, а следовательно, и неразличимы. Различить отдельные атомы? Это прежде казалось утопией, абсурдом!
Теперь иное. Изотопы (их способность метить атомы и молекулы) стали мощнейшим оружием ученых. Они позволили наконец заглянуть в святая святых растительной клетки и понять, что значит в ней Светлое и Темное.
5
В 1929 году два американских химика У. Джиок и X. Джонсон обнаружили, что кислород представляет собой смесь трех изотопов: О16, О17 и О18.
Наиболее распространен кислород О16: из каждых 10 000 кислородных атомов 9976 приходится на Ои (8 протонов и 8 нейтронов), 20 - на О18 (8 протонов и 10 нейтронов) и лишь 4 атома - на изотоп О17 (8 протонов и 9 нейтронов).
Естественно - в качестве метки выбрать кислород О18, он сильнее отличается от "эталонного" изотопа О16, кроме того, он все-таки в пять раз чаще встречается, чем О17, а добывать тяжелые изотопы кислорода ох как нелегко!
Воду, обогащенную кислородом О18, получают электролизом.
В этом процессе (пропускание электрического тока через воду) в молекулах воды.рвутся химические связи между атомами кислорода и водорода.
Однако чем молекулы массивнее (вода с О17 и О18), тем связь крепче, порвать ее труднее. Потому-то при электролизе и происходит накопление молекул воды с изотопами О17 и О18.
Так, после долгих и утомительных трудов, как награду, удается получить воду с достаточно высоким процентным содержанием изотопа О18.
В 1941 году группа американских химиков, возглавляемая С. Рубеном и М. Каменом, пропела решающие опыты. Водорослям дал PI "попробовать" водички, предварительно обогащенной изотопом О18.
И тут же растительные клетки начали выделять кислород, в котором концентрация О18 была также аномально высокой.
Но это было еще не все. Теперь исследователи пометили углекислый газ (его специально готовили, окисляя атомы углерода тяжелым кислородом О18).
Когда меченый углекислый газ дали водорослям (вода при этом, естественно, оставалась непомеченной), то кислород, образующийся в процессе фотосинтеза, никак не "реагировал" на это воздействие.
Да, теперь уже сомнений не было: источником кислорода в растениях (подобные опыты стали проводить и с ними) явилась вода, а вовсе не углекислый газ, как полагали, прежде.
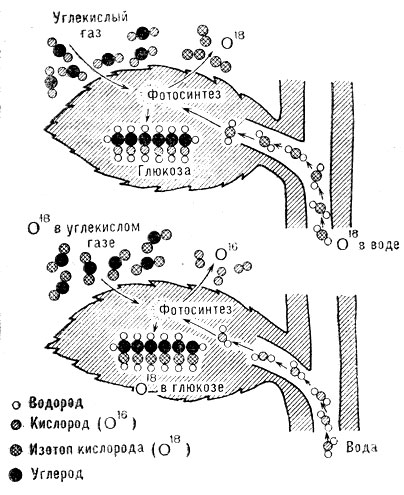
Применение изотопа кислорода (О18) показывает, что в процессе фотосинтеза для построения молекулы глюкозы растение использует кислород из углекислого газа, а не из воды
Как легко и доказательно (буквально в два счета) решила новая изотопная техника уже столетие длившийся спор исследователей. Формальдегидная теория Байера, еще вчера казавшаяся такой незыблемой и надежной, рухнула в один миг.
Природа в процессе фотосинтеза избрала не более простой и естественный, как казалось теоретикам, путь, а более сложный, сообразуясь с правилами игры, которые мы еще подчас просто не понимаем.
6
Виноградов (1895-1975), советский геохимик, академик (1953), вице-президент Академии наук СССР (1967), Герой Социалистического Труда (1949), директор Института геохимии и аналитической химии имени В. И. Вернадского (с 1947), член международной Пагуошской конференции ученых - защитников мира (с 1958), награжден пятью орденами Ленина. Окончил Военно-медицинскую академию и химический факультет Ленинградского университета (1924); как и его учитель Вернадский, вел исследования широчайшего диапазона (Вернадский, как известно, создал по меньшей мере три науки: геохимию, биогеохимию и радиогеологию) - от биогеохимии до космохимии. Изучал закономерности распределения химических элементов в земной коре, определил абсолютный возраст Земли, непосредственно участвовал в создании атомной промышленности, изучал состав метеоритов, занимался проблемами химии планет (открыл базальты - вулканические породы - на поверхности Луны, определил состав атмосферы Венеры), под его руководством исследовались образцы лунного грунта, доставленные космическими аппаратами, широко и успешно применял разнообразные изотопные методы (создал новое для науки СССР направление - геохимию изотопов).
Вопрос о происхождении кислорода в растительной клетке был решен одновременно двумя группами исследователей.
1941 год. Войска Гитлера рвутся к Москве, на окраинах женщины и подростки строят укрепления. Бомбежки, ночные дежурства...
И в это же время в одном из тихих переулков Москвы (Старомонетном), в Биогеохимической лаборатории Академии наук СССР велись удивительные для тех суровых времен опыты.
Александр Павлович Виноградов (будущий академик) и сотрудница лаборатории Руфина Владимировна Тейс выпытывали у растений: чей же, собственно, кислород они выделяют в атмосферу?
Методика работы советских ученых отличалась от американской, но суть была та же - использовать чудесные свойства изотопов.
Советские ученые воспользовались тем обстоятельством, что, оказывается, в углекислом газе тяжелых изотопов кислорода больше, чем в воде.
Надо было сравнить изотопный состав воды, углекислого газа и выделяемого растениями кислорода. Исследования показали "родство" кислорода и воды. Значит, вывод получается гот же, что и у американцев (открытие было сделано одновременно): растения извлекают кислород из воды, а не из углекислого газа.
Вскоре аналогичные опыты с использованием самой совершенной аппаратуры стали проводить и в иных местах - в лабораториях Лондона, Токио и других городов мира.
Результаты были неожиданными.
Нет, исследования Рубена и Камена, Виноградова и Тейс не были опровергнуты: в основном кислород, видимо, брался растениями из воды. Однако изотопный состав этих веществ (воды и кислорода) все же не совпадал полностью.
Это и был сюрприз.
Содержание О18 в кислороде изменялось от опыта к опыту. Возникло подозрение: часть кислорода все же отщепляется и от углекислого газа. Процентов этак от 15 до 30.
Ученые разбились на оптимистов, сторонников водного происхождения кислорода (они старались не замечать новые факты), пессимистов, злорадно выглядывавших из-под обломков формальдегидной теории Байера, и скептиков - эти просто ехидничали по поводу самых последних научных новостей: дескать, состав кислорода, конечно же, должен зависеть от того, на каком континенте проводятся опыты, в какой стране...
Почти 20 лет шло научное препирательство. Никто толком ничего не понимал, пока, наконец, в 1960 году тот же Виноградов (уже академик) вместе со своим сотрудником Владимиром Михайловичем Кутюриным не внес в это дело решающую ясность.
Все-таки кислород растения получают из воды.
А причина недоразумений крылась... в дыхании растений.
Дыхание у растений переменчиво, зависит от многих факторов и условий. Потому и изотопный состав кислорода в опытах был неустойчив (та невоспроизводимость, над которой так потешались скептики).
Ну а вот почему в кислороде тяжелых изотопов больше, чем их содержится в "материнской" воде, - тут ответ был удивителен. Растениям, оказывается, "по вкусу" (при дыхании они поглощают кислород) не любой изотоп кислорода, они отдавали явное предпочтение самому легкому - изотопу О16.
Ученые установили также: чем хуже чувствует себя растение, тем более оно разборчиво, прихотливо но отг ношению к самому из реакционноспособных среди изотопов кислорода - только О16.
Кто знает, может быть, это один из методов будущей диагностики человеческих болезней? Ведь, скорее всего, как и у растений, организм человека также, видимо, должен предпочитать изотоп О16. И тем строже, чем человек слабее...
Итак, дело происходит в растительной клетке следующим образом.
Растение извлекает кислород из воды, и тут изотопный состав кислорода газообразного и кислорода, содержащегося в исходной воде, конечно, одинаков. Но затем в этот процесс вмешивается дыхание, смазывая всю картину.
Растение, словно лакомка, отбирает преимущественно легкую фракцию изотопов кислорода, в результате остающийся кислород утяжеляется: тяжелых изотопов в нем становится больше.
Вот она, разгадка!
Так в длящемся почти целый век споре исследователей была наконец поставлена последняя точка. И сделали это советские ученые.
7
Новая экспериментальная техника (мы уже убеждались в этом не раз) решает если не все, то многое.
Никакие даже самые чувствительные весы не уловят разницу между стабильными изотопами, скажем О16 и О18. Тут нужны особые устройства: ими стали масспектрометры.
Действуют эти приборы так. Прежде всего исследуемое вещество переводится в газообразное состояние. Затем его ионизируют, обстреливая из "электронной пушки". После поток полученных ионов направляют в магнитное поле (в камере, где создан высокий вакуум). Здесь изотопы и разделяются: ионы разного веса (О16 и О18) движутся в магнитном поле по разным траекториям: чем легче ион, тем он сильнее отклоняется от первоначального пути.
Так, наконец, получается искомый спектр масс.
Все значительно проще с изотопами радиоактивными. Тут каждый "взрывающийся" атом может обнаружить, проявить себя. К примеру, в портативном и простом в обращении счетчике Гейгера - Мюллера.
Надобность в достаточно больших количествах анализируемого вещества отпадает.
Другое достоинство радиоизотопов - за ними можно вести слежение на всех этапах исследуемого процесса, изучая не только вещества на "входе" и "выходе", но и промежуточные звенья долгой цепи превращений.
Дешевизна, точность, быстрота, простота все говорит за радиоизотопы.
Посмотрим же, что нам тут приготовила Природа.
Начнем с водорода.
У него радиоактивен только тритий: самый тяжелый изотоп, обнаруженный в 1939 году.
Водород - участник очень многих процессов в клетке. Но, к сожалению, он и самый подвижный из атомов: скачет от молекулы к молекуле, словно молодой лягушонок, охотно меняя места.
Как метка, индикатор он бесполезен. Ведь метка ценна, если она крепко "привязана" к какому-то центру, узлу клетки, помечая, выделяя его... Скачущая же метка не имеет никакой цены.
Обратимся теперь к кислороду. Кроме стабильных изотопов О16, О17 и О18, известны и нестабильные изотопы: О14, О15, О19. Можно ли их использовать? Увы, нет! Все радиоактивные изотопы различаются периодом полураспада: тем временем, в течение которого половина исходных атомов выйдет, так сказать, из строя, развалится. Период полураспада урана - 238 4 510 000 000 лет. А у изотопов О14, О15 и О19 всего лишь соответственно 1,23; 2,05, 0,50 минуты. За такое время ничего-то не успеешь сделать! Нет, для исследований фотосинтеза эти метки также непригодны.
Но у нас. еще в запасе атомы углерода: проследить путь углекислого газа в растительных клетках - об этом мечтали многие поколения ученых.
Кроме стабильных изотопов углерода С12 и С13, в конце 30-х годов, уже были известны и радиоактивные. Наибольшим долгожителем среди них был изотоп С11, с периодом полураспада примерно в 20 минут.
Не так уж и много, но и не так мало, кое-что можно успеть.
Углерод - элемент необычный. Это ключевое вещество жизни, состоящей преимущественно из углеродных соединений.
Уникальность углерода обусловлена его свойствами, которыми в совокупности не обладает ни один другой элемент периодической системы (и даже очень похожий на углерод кремний): способностью легко образовывать прочные связи с одним, двумя, тремя, четырьмя элементами, но эти связи, однако, в случае нужды также легко могут быть разорваны, склонностью к построению длинных цепей, циклов - этих "скелетов" всего живого...
Собственно, само возникновение жизни на Земле - это мучительный и сложный процесс эволюции углеродных соединений.
Да, углеродные радиоактивные метки были бы для ученых большим подарком, счастливым шансом.
1940 год. Радиационная лаборатория Калифорнийского университета. Уже известные нам С. Рубен и М. Камен и их сотрудники с помощью изотопа С11 исследуют фотосинтез.
Трудное это было дело! Ведь через 20 минут в ваших руках останется лишь половина исходных атомов-меток, через час - восьмая часть, через два часа - 1/64 и так далее. Изотопы тают на глазах, словно лед.
И за эти два-три часа надо успеть сделать так много: синтезировать радиоактивный углекислый газ (меченый), ввести его в растение, в котором произойдут различные метаморфозы исходного радиоактивного углерода...
Требовалась дьявольская изворотливость, быстрота, необходимо было работать без ошибок.
Радиоизотопы в те времена были еще очень дороги, редки и крайне опасны в обращении. Рискуя здоровьем, подвергаясь многократному облучению (техника защиты от радиации тогда только делала свои первые шаги), работали ученые.
Труд был опасен и тяжел, а результаты очень скромные.
Было показано, что вопреки предсказаниям углекислый газ присоединялся не к хлорофиллу, а к какому-то сложному органическому соединению с молекулярной массой, примерно равной тысяче.
Но самый досадный результат - то, что, как показали эти опыты, уже через считанные минуты радиоактивная метка обнаруживалась сразу в десятках мест. И было очевидно, что эти различные меченые молекулы в свою очередь в живой клетке "растворены" в тысяче других молекул, уже не радиоактивных.
Значит, требовалось отделить, так сказать, "плевелы от пшеняцы": меченые молекулы - от остальных. И тут требовались не только изощренные биохимические приемы, но и немалое время!
И с изотопом С11 этого было сделать нельзя.
8
До зарезу нужен был долгоживущий радиоактивный изотоп углерода.
В 1939 году Мартин Камен вместе с Сэмюэлехм Рубеном начал систематическое опробование методов, которые позволили бы синтезировать искусственный радиоизотоп С14.
(Их не смутило, что атомная теория тех времен предрекала этому изотопу очень краткие сроки жизни.)
И в 1940 году пришел успех.
Ученые бомбардировали углерод С12 дейтерием и получили радиоизотоп С14.
К великому изумлению и не менее великой радости, этот изотоп неожиданно оказался долгожителем - период его полураспада 5 770 лет.
Природа на сей раз была благосклонна к исследователям.
Пять тысяч лет - срок достаточно долгий: теперь можно было следить за любым, даже самым "неповоротливым" процессом, идущим в живой ткани. И в то же время этот период полураспада был и не слишком длинен: число распадов в единицу времени оказалось достаточно большим, их удавалось уловить с помощью существовавших тогда приборов (а ведь можно вообразить и столь медлительный радиоактивный процесс, такой, что его просто трудно обнаружить!).
Углерод С14 изменил лик биохимии: с его "легкой руки" было сделано не одно важное открытие...
Удача, говорят, не приходит одна.
В 1944 году два английских биохимика - Арчер Мартин и Рихард Синг - радикально усовершенствовали хроматографический метод, созданный в начале этого века русским ученым Михаилом Цветом для разделения пигментов и других смесей молекул.
Хроматография старая, в колонках с порошкообразными адсорбентами - мелом, сахарной пудрой и тальком, имела ряд недостатков: количество анализируемого вещества (оно распределялось в колонке в виде узких колец) должно было быть немалым, трудоемкой оказывалась процедура извлечения, то есть вымывания нужных компонентов из пор колонки.
Мартин и Синг заменили колонку... промокашкой, специально подобранной фильтровальной бумагой.
И сложное стало простым.
Теперь анализ шел таким образом.
На полоску фильтровальной бумаги (в один из уголков) наносили каплю раствора: в ней была смесь подлежащих разделению веществ.
Затем после просушки этот же уголок опускали в растворитель. Двигаясь по бумаге, увлекаемый капиллярными силами, растворитель несет с собой и части анализируемой смеси: и каждая компонента оседает на листке в разных местах.
Теперь осталось только проявить хроматограмму: обработать листок бумаги химикалиями, дающими во взаимодействии с разными веществами смеси различные цветовые реакции. И, словно перья павлина, листок расцвечивается ярким узором: каждая составляющая смеси как бы расписывается на нем...
(За это изобретение в 1952 году Мартин и Синг были удостоены Нобелевской премии по химии.)
И еще один необычно удобный метод исследований вскоре оказался в руках ученых - авторадиография.
Ведь радиоактивное излучение оставляет след на эмульсии фотопластинки, радиоизотопы способны как бы сами себя сфотографировать, так что можно проследить, в каких именно клетках или клеточных структурах преимущественно оседает радиоактивный изотоп, локализуется то или иное вещество.
(К примеру, таким путем физиологи растений узнали, куда уходят фосфор и сера, содержащиеся в известном удобрении - суперфосфате. Для этого к суперфосфату добавили радиоактивные фосфор Р32 и серу S35. Картину распределения этих элементов затем просто сфотографировали, получив нечто вроде рентгеновского снимка.
Результат? Фосфор и сера в основном идут в листья растений, туда, где происходит процесс фотосинтеза.)
...В середине 40-х годов ученые, изучающие фотосинтез, владели всем необходимым: можно было смело приступать к решающей атаке и попытаться выяснить пути превращения в растении углекислого газа.
Но шла жестокая война с фашизмом. В Калифорнийском университете исследования были свернуты.
Кроме того, в результате несчастного случая у себя в лаборатории погиб признанный лидер этих исследований - Сэмюэль Рубен...
9
Кальвин, родился в 1911 году, американский биохимик, сын русского иммигранта, окончил Мичиганский колледж горного дела и технологии (1931), с 1937 года - в Калифорнийском университете. С 40-х годов работает над проблемами фотосинтеза. Вместе с возглавляемой им группой исследователей в 1946-1957 годах изучал идущие в растительной клетке темновые процессы, в результате которых углерод углекислого газа откладывается в растениях в виде Сахаров и других веществ. За расшифровку этого цикла превращений (восстановительный карбоновый цикл, или просто цикл Кальвина) ученый в 1961 году был удостоен Нобелевской премии по химии. Кальвин известен также своими работами по химической эволюции (происхождение жизни на Земле) и новыми идеями по использованию растений как источников энергии.
Эстафету научного поиска в послевоенные годы подхватила другая группа исследователей того же Калифорнийского университета.
Возглавил ее Мелвин Кальвин, 35-летний биохимик.
В 1946 году он сформировал в основном из выпускников Калифорнийского университета (теперь это известные ученые: Дж. Бассам, Э. Бенсон и другие) новую команду и поставил цель - проследить в растительной клетке судьбу меченых углеродом С14 молекул углекислого газа.
Вначале приемы работы были незатейливы. Брали лист растения, помещали его в камеру с меченым углекислым газом, выжидали некоторое время (конечно, лист был освещен: в нем шел процесс фотосинтеза), а затем лист погружали в спирт.
Эта мера, по мысли ученых, должна была остановить течение биохимических процессов в листе, "заморозить" их на какой-то вполне определенной стадии.
И тут возникло первое осложнение. Мгновенно "убить" лист, сразу и одновременно выключить, как свет в комнате, все процессы в нем никак не удавалось. Пока этот спирт проникнет в лист... дойдет до центров фотосинтеза - хлоропластов!.. Несколько секунд вроде бы немного, но за это время успевает совершиться множество биохимических реакций, меченые углеродом продукты фотосинтеза по инерции вступают в новые связи с другими молекулами, стройная картина фотосинтеза оказывается смазанной...
Не сразу созрела спасительная мысль: взять объектом исследований одноклеточную водоросль - хлореллу.
Эту крошку (ее едва удается разглядеть в обычный микроскоп) уже можно разрушить одним, так сказать, ударом: спирт (расстояния малы: диффузия идет быстро) тотчас выводит из строя ее ферменты, дезактивирует их, и процесс фотосинтеза замирает.
Теперь исследователям предстояло выяснить, какие же химические соединения в "замороженной" клетке хлореллы окажутся помеченными углеродом С14.
И вновь - проблемы! Уже через минуту радиоактивный изотоп составлял часть "плоти" по крайней мере 15 различных молекул. Среди них были не только сахара, но и аминокислоты - составные части белков.
Ученые попали в настоящие биохимические джунгли: заблудиться в них было очень просто.
Оставалось одно - максимально сокращать время до того момента, когда процесс фотосинтеза останавливается. До секунд и даже долей секунды. Только тут была надежда обнаружить самые первые продукты фиксации 14С02 - меченого углекислого газа.
Работу группы Кальвина смело можно сравнить с археологическими раскопками. По отдельным меченым молекулам предстояло восстановить всю сложную цепь, последовательность фотосинтетических превращений.
Исследователи убивали хлореллу, дробили ее клетки в центрифугах, с помощью бумажной хроматографии Мартина и Синга разлагали молекулярные смеси на составляющие, идентифицировали их, а авторадиография указывала те молекулы, где в момент остановки фотосинтеза "застревал" меченый углерод.
По мнению Кальвина и его сотрудников, самым первым продуктом фотосинтеза оказалась (конечно же, не формальдегид! Акции этой почтенной теории давно уже котировались довольно низко, теперь же она и вовсе тихо сошла с научной сцены) фосфоглицериновая кислота.
Вот ее химический портрет:
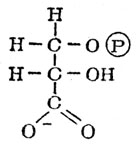
В ней три атома углерода (С), атом фосфора (Р) водород (Н) и кислород (О).
И снова загадки. Чтобы из молекулы углекислого газа С02, содержащей один атом углерода, получить трехуглеродные соединения, требовался двух - или хотя бы одноуглеродный предшественник. Но вот его-то никак не могли найти.
Зато обнаружили довольно сложные пяти - и даже семиуглеродные соединения.
Долго и непросто вспоминать все перипетии исследований (они длились целое десятилетие) Кальвина и его многочисленных сотрудников. Как, когда, с каким трудом был преодолен каждый барьер, устранены "подводные камни", нащупаны, наконец, верные пути.
Изложим сразу конечные результаты - то, что сейчас в энциклопедиях, монографиях, учебниках стало историей науки и фигурирует под многими "вывесками": углеродный цикл, цикл Кальвина, цикл регенерации рибулозодифосфата.
Принцип работы этого цикла в следующем: углекислота прежде всего связывается с акцептором (по биохимической терминологии это слово означает вещество, принимающее в свой состав различные атомы или атомные группы) рибулозодифосфатом. Или кратко - РДФ (биохимикам трудно обойтись без сокращений).
Эта молекула, давшая циклу одно из его имен, имеет вид:
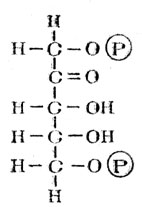
В ней пять атомов углерода и два атома фосфора.
Соединяясь с молекулой углекислого газа, РДФ образует уже шестиуглеродное соединение, которое затем разваливается, распадается на две трехуглеродные (вот она разгадка!) молекулы фосфоглицериновой кислоты (смотри выше).
Далее следует сложная цепь превращений, в которую включается и отщепленный от воды водород (мы помним, что на свету растение расщепляет воду, выделяя в атмосферу кислород). Образуются последовательно триозофосфат, гексозофосфат и сахара - конечные продукты, выходящие из цикла.
Часть же промежуточных соединений сложными путями возвращается в цикл. Что и приводит к регенерации исходного РДФ.
И восстанавливается исходная позиция этого биохимического танца. Цикл готов прокрутить еще один оборот: обновленная молекула РДФ готова принять новую, только что поступившую из воздуха молекулу углекислоты.
(Мы обрисовали - и довольно грубо - лишь основной каркас, скелет этого замечательного процесса. Умолчали о многих существенных деталях, о деятельности разнообразных ферментов, участвующих в цикле, о целом комплексе условий, обеспечивающих исключительно тонкую настройку всего этого механизма.)
Позже было доказано: цикл Кальвина успешно действует не только в хлорелле, но и в хлоропластах высших растений и во многих других способных к фотосинтезу живых объектах.
В заключение отметим важное обстоятельство.
Все биохимические превращения цикла Кальвина (это доказано) могут идти в полной темноте. Между тем для образования Сахаров и других продуктов из углекислого гвзш и воды требуется энергия. И немалая. Откуда она берется?
Растениям дает энергию свет, подскажет читатель. И будет прав, но лишь наполовину. Ибо остается неясным, какие пертурбации испытывает квант света, в какой форме его энергия доходит до углеродного цикла.
Мы возвратились к тому, с чего начали.
Усилия Кальвина и его сотрудников сделали темное светлым! Идущие в растениях темповые процессы фотосинтеза стали более или менее понятны. Но вот светлое? Смысл этой стадии фотосинтеза, ее подробности пока остаются для нас загадочными.
Это и есть тема дальнейшего рассказа.
(Заметим, что и сейчас даже для профессионалов, занимающихся фотосинтезом, светлое по-прежнему полно таинственности, и "светлить" эту стадию будет еще, видимо, не одно поколение ученых.)
10
Теренин Александр Николаевич {1896-1967), советский физико-химик, академик (1939), Герой Социалистического Труда (1966), родился в Калуге (знал Циолковского лично, но ни космонавтикой, ни авиацией не увлекся), в 1914 году учился в Петрограде в Психоневрологическом институте (заинтересовавшись проблемами интеллекта и контактов между людьми, хотел было даже стать режиссером, но в конце концов увлекся молекулами, осознав, что с ними можно разыгрывать не менее яркие "спектакли", чем с актерами!), окончил Петроградский университет (1922) - одновременно с учебой работал с 1919 года в только что созданном Оптическом институте лаборантом при мастерских (его руководитель будущий академик Д. С. Рождественский, давая ему первую тему для студенческой работы, писал в записке: "До Вас этой темой безуспешно занимались уже два Александра Николаевича - Заборовский и Захарьевский. Вы - третий. Постарайтесь дотянуть чувствительность фотопластинки до длины волны в 1 микрон, где находится линия спектра ртути. Вот Вам последние остатки импортного дицианина, позволяющего на пределе достигнуть длины волны в 0,9 микрона, но расходуйте его только в случае крайней необходимости. Желаю Вам успеха". Наметив столь мрачные перспективы предстоящей работы, Рождественский отбыл в длительную заграничную командировку. Уже в этой первой своей научной работе Теренин проявил блестящее мастерство экспериментатора. Не потратив и грана драгоценного дицианина, он нашел нестандартное решение. Его выводы исправили ошибочные результаты Мак Леннана). Теренин проработал в Государственном оптическом институте почти 50 лет (руководил им в 1945-1956 годах), одновременно вел кафедру в Ленинградском университете. Главная тема работ Теренина - воздействие света на вещество, им владело страстное желание решить проблему химического использования энергии Солнца. (В 1964 году на Международном конгрессе по фотобиологии, представляя Теренина, профессср Боуэн так его характеризовал: "...доктор Теренин сам есть устойчивое, крайне энергетичное, активное и ярко светящее состояние материи...") Теренин создал большую школу советских фотохимиков, наука для него была единственной целью и главным смыслом жизни (уже тяжело больной, находясь в больнице, он потребовал пристроить к кровати специальный пюпитр, на котором писал последнюю книгу "Фотоника молекул красителей"). Инициатор создания Института фотосинтеза Академии наук СССР, был первым председателем Научного совета Академии наук СССР по фотосинтезу, награжден четырьмя орденами Ленина, Государственной премией СССР (1946), Золотой медалью имени С. И. Вавилова (1953) за работы по люминесценции.
Энергию растению дает свет - это теперь азбука. Но как все происходит?
Прежде всего, как молекулам удается поймать и - главное - удержать энергию световых лучей? Удержать (ведь хлорофилл может высветить энергию, и она потратится "пустую) достаточное время, в течение которого будут реализованы полезные для растения процессы.
Если на минуту отвлечься от проблемы собственно фотосинтеза и взглянуть на дело широко, то все пигменты, которыми наполнены хлоропласты растений, предстанут перед нами как рядовые великой армии красителей.
Среди многообразных соединений органической химии красители выделяются интенсивным поглощением видимого света. Это и обусловливает их яркие цвета (поэтому их и используют с давних времен для крашения).
Но, кроме эстетики, тут кроется и глубокая физика: красители - мощные приемники солнечной радиации, именно они способны превращать ее в иные формы.
Теренин, всю жизнь изучавший взаимодействие света и вещества, не мог не увлечься красителями и пигментами. Эта тема на долгие годы становится одной из ведущих на его фотохимических семинарах.
Как происходят элементарные фотопроцессы в молекулах красителя? Как создать искусственные системы для эффективного химического использования солнечного излучения, системы, способные конкурировать с естественными?
Это была очень сложная и величественная программа исследований (весь спектр: от простейших моделей до хлорофилла и его аналогов, от искусственных моделей до изучения живых хлоропластов) в очень трудной области.
Работа спектроскописта во многом похожа на деятельность криминалиста. Спектр вещества, его "паспорт", содержит богатую и ценную информацию о строении молекулы красителя, о его взаимодействии со светом. Чтобы расшифровать спектры, необходимо сопоставить различные спектральные характеристики большого ряда родственных соединений. Дело это трудное: даже для простейшего ароматического соединения - бензола интерпретацию электронного спектра еще нельзя считать законченной.
Что же скрывается за спектром, какие процессы?
Тут нам не обойтись без физики, которая доказала двойственную природу света: это и электромагнитная волна и поток световых квантов - фотонов.
Каждый фотон несет сгусток, порцию, квант энергии. Хотя по нашим обыденным меркам энергия отдельного кванта света и ничтожна, для молекулы, поглотившей фотон, - это "крупное событие". Квант коротковолнового ультрафиолетового света вызывает в молекуле красителя такие разрушения, что его действие можно сравнить с последствием прямого попадания в цель крупнокалиберного снаряда.
Замечательное свойство фотосинтеза в том и состоит, что растения умеют продуктивно использовать такие мелкие (в сравнении с ультрафиолетом) порции энергии, как кванты красного света, присутствующие в большом количестве в солнечной радиации.
Умение это отличает хлорофилл, атомы которого под действием света начинают вибрировать, давая характерные спектры излучения и поглощения (с ними и колдуют спектроскописты).
Молекула красителя способна поглотить только один фотон. При этом она приходит в так называемое возбужденное состояние. Это значит, что один из ее электронов изменяет свой статус: перескакивает на более высокий энергетический уровень.
Энергия поймала - теперь ее надо удержать. По-дольше.
Тут начинаются варианты: возбужденное состояние молекулы называется синглетным, если переход электрона вверх по энергиям не сопровождается изменением знака его спина (от английского spin - вращаться, вертеться) - характеристики его собственного момента импульса.
Синглетному состоянию (или просто синглету) в спектре поглощения соответствует лишь одна линия (отсюда и английское название single - "один", "единственный").
Другой вариант - триплетное состояние возбужденной молекулы. Теперь электрон при переходе меняет знак спина (волчок переворачивается вниз головой!). В спектре появляются не одна, а сразу три характерные линии (отсюда и название - триплет).
Синглет и триплет различаются и временем жизни. Синглетные молекулы живут в возбужденном состоянии очень мало, примерно 10-9 секунды, а триплетные уже порядочно, 10-3 секунды (разница на шесть порядков).
В 1943 году Теренин обосновал ныне общепринятые представления о том, что у молекулы хлорофилла фотохимически активным состоянием является именно долгоживущее триплетное состояние. Что молекула хлорофилла (ее порфириновое кольцо) так и "сконструирована" специально природой: в триплетном состоянии (для молекулы время 10-3 секунды не так уж мало) хлорофилл может удержать энергию кванта света достаточно долго, чтобы смогла совершиться ее дальнейшая утилизация.
(Годом позже, в 1944 году, американский физико-химик Дж. Льюис независимо от Теренина высказал ту же мысль. Любопытно, что после окончания войны, ознакомившись с советскими работами, Льюис обратился к Теренину с письмом, в котором признавал его приоритет.)
Обычный зеленый хлорофилл (это его основное состояние) довольно малоактивное вещество. Однако возбужденный светом хлорофилл совершенно не похож на этот зеленый пигмент. Даже его окраска в триплетном состоянии изменяется: он становится красно-коричневым (мы этого не замечаем, так как неспособны уследить за процессами, протекающими за 10-3 секунды).
Изменение цвета хлорофилла было доказано, когда применили особую импульсную спектроскопию: она и позволила измерить спектр поглощения триплетных молекул.
Превратившись из зеленого в красно-коричневый, перейдя в свое активное, рабочее состояние, хлорофилл готов действовать дальше.
Что значат эти слова? Об этом сейчас и пойдет речь.
11
Сент-Дьердьи, американский биохимик, по национальности венгр, родился в 1893 году в Будапеште в семье известных ученых, з первую мировую войну служил в австрийской армии (был награжден за храбрость, но, не видя смысла в этой бойне, совершил самострел и вернулся к учебе), окончил Будапештский университет (доктор медицины, 1917), затем продолжение учебы (его родители, аристократы, к тому времени были разорены, и он был вынужден жить самостоятельно) и научная работа в Нидерландах, Великобритании, США. В 1930-м вернулся в Венгрию (президент университета в Сегеде, в 1944-м участвовал в Движении Сопротивления), гражданин США с 1955 года. Выделил из растительных и животных тканей аскорбиновую кислоту и показал ее идентичность витамину С (Нобелевская премия по медицине и физиологии, 1937), изучал (автор ряда теорий) механизмы Мышечного сокращения. Член Национальной академии США (1956) и Американской академии искусств и наук (1957), иностранный член Академии наук СССР (1947), почетный член Венгерской академии наук (1945).
В книге "Биоэнергетика" (1957) Альберт Сент-Дьердьи писал: "Проблема ставится так: каким образом энергия управляет жизнедеятельностью? как она приводит в движение живую машину?"
Специально фотосинтезом Сент-Дьердьи никогда не занимался, но последние десятилетия (особенно показательна здесь его книга "Биоэлектроника", 1968) он неустанно размышляет над путями преобразования энергии в живых клетках.
Итоговая, суммарная картина фотосинтеза ясна. Энергия света перестраивает химические связи в исходных молекулах - углекислого газа (С02) и воды (Н2О). Вместо прежних связей "углерод - кислород" и "водород - кислород" возникает иной тип химических связей: "углерод - водород" и "углерод - углерод".
Схематически на языке химии это можно изобразить так:
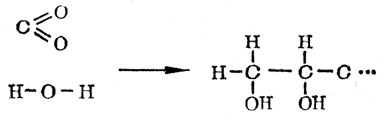
Этот процесс образования углеводов (цикл Кальвина) идет в темноте; следовательно, свет тут вроде бы ни при чем. Откуда же берется энергия?
Разъяснение (принцип, общий подход к вопросу) дает Сент-Дьердьи: "С какой бы стороны мы ни пришли к биологии - со стороны ли материи или со стороны энергии, - мы так или иначе придем к электронам. Удивительно тонкие биологические реакции, по всей вероятности, представляют собой реакции очень мелких лабильных единиц, каковыми являются электроны".
Дело происходит так.
Поглотив фотон красного света, хлорофилл переходит в возбужденное триплетное состояние. Обладающий избытком энергии один из электронов этой молекулы по специальной хитро устроенной цепочке ферментов ("цепь электронного переноса" - так ее называют), покинув хлорофилл, "уходит" в цикл Кальвина.
Потеряв электрон, хлорофилл оказывается заряженным положительно; в нем образуется, как образно выражаются физики, электронная "дырка".
Это вакантное, привлекательное (разноименные заряды притягиваются) для электронов место в результате каких-то пока еще полностью не изученных процессов "затыкает" электрон одной из ближайших молекул воды.
Вода при этом разваливается: ее кислород выделяется в атмосферу, а оставшийся протон устремляется в цикл Кальвина.
Молекула же хлорофилла, вернув потерянный прежде электрон, возвращается в исходное, зеленое состояние. Она готова к новому циклу.
Превращения хлорофилла (поглощение фотона, потеря и возвращение одного из электронов), составляющие суть светлой стадии, - это все процессы быстрые. Поэтому эта стадия фотосинтеза идет довольно скоро, за малые времена (вспомним работу Эмерсона и Арнольда).
Напротив, миграция электрона (покинувшего молекулу хлорофилла) и протона (осколок молекулы воды) в цикл Кальвина, свершение в этом цикле длинного ряда биохимических процессов - все это требует уже гораздо большего времени.
Поэтому темное во времени растянуто гораздо больше, нежели светлое.
Мы снова упростили реальную картину, обрисовав лишь ее скелет, совсем не касаясь многих тонких вопросов, подлежащих компетенции новой области биологии - квантовой биохимии (ее основателем считается Сент-Дьердьи). Квантовая биохимия, представляющая собой приложение законов современной квантовой механики к вопросам биологии, ведет анализ на субмолекулярном уровне, на уровне электронных взаимодействий.
Этот подход оказался очень плодотворным. Но его обсуждение завело бы нас очень далеко от того, к чему мы сейчас стремимся - понять то основное, что и составляет суть световой стадии фотосинтеза.
12
Арнон, родился в 1910 году, американский биохимик и физиолог растений, по происхождению поляк, окончил Калифорнийский университет (1932), с 1936-го преподает в нем, известен работами по фотохимии хлорофилла в растениях и в извлеченных из них хлоропластах, в 1954 году открыл процесс фотосинтетического фосфорилирования.
Мы все-таки ушли от ответа: как же энергия электрона преобразуется в энергию химических связей? Но этого в подробностях пока еще вообще никто не знает. Понятна лишь такая аналогия. Электроны, эти движители жизни, достигают в молекуле хлорофилла (после поглощения ею кванта света) высокого энергетического состояния. Они как бы взбираются на высокую горку.
С этого высокого энергетического уровня электроны скачками, как скатывающийся по лестнице шар, спускаются на более низкие уровни.
Жизнью движет энергия, отдаваемая электронами на каждой ступеньке этой лестницы.
И опять (в который раз!) - вечный круговорот. Квант света поднимает электрон вверх по лестнице, затем он (электрон) самопроизвольно спускается вниз, даря энергию всему живому; после новый фотон вздымает электрон (уже другой)... И так до бесконечности.
Но ночью солнце не светит, а энергия нужна клеткам постоянно. Как быть? Природа, оказывается, решила и эту задачу. Она научилась консервировать энергию бегущих вниз электронов, откладывать их про запас.
В растениях этот процесс носит длинное и малопонятное название - фотосинтетическое фосфорилирование. Открыл его в 1954 году Даниел Исраэл Арнон.
Этот ученый осуществил-таки мечту академика Фаминцина: заставил "жить" обособленно выделенные из растительной клетки хлоропласты, эти клеточные органеллы, целиком специализирующиеся на фотосинтезе.
Многие ученые пытались заставить функционировать изолированные хлоропласты. В 1937 году большого успеха добился англичанин Р. Хилл. Его хлоропласты при освещении выделяли кислород. Но поглощать углекислый газ упорно отказывались.
Изолированные хлоропласты оказались очень капризным объектом. Их выделяют обычно (стандартная процедура) из листьев шпината.
Даже начальные стадии выделения хлоропластов - растирание листьев и их промывание - требует большой осмотрительности: среда должна быть щелочной, содержать сахарозу и ионы хлора. Важно также было добиться, чтобы хлоропласты не старели быстро: ие теряли свою фотосинтетическую активность. Тут также нужны особые условия - соответствующая температура, присутствие ионов магния и так далее.
"Ублажив" хлоропласты полностью, Арнон в 1954 году одержал полную победу: его изолированные хлоропласты исполняли весь фотосинтетический цикл превращений, целиком! Отныне ученые, изучающие фотосинтез, могли экспериментировать не с растительными клетками, а с отдельными хлоропластами, что было гораздо удобнее и давало больший научный "урожай".
Арнон показал, что хлоропласты сами снабжают себя энергией, что в них идет процесс фотосинтетического фосфорилирования.
Чтобы понять смысл последней фразы, прежде всего расшифруем слово "фосфорилирование". Оно означает образование богатой энергией (макроэргической) фосфатной связи в молекуле аденозинтрифосфата (сокращенно: в молекуле АТФ).
Идет химическая реакция:
АДФ + Ф = АТФ.
Аденозиндифосфат (АДФ) соединяется с еще одним фосфатом (Ф), образуя АТФ (соединение с двумя - ди! - фосфатными связями присоединяет третью, высокоэиергетическую химическую связь).
Молекула АТФ - энергетическая "валюта" любого организма (от микроба до человека). Любой процесс в клетке черпает энергию из молекул МФ (из ее третьей фосфатной связи). Энергия выделяется, когда АТФ расщепляется (обратная реакция) на АДФ и Ф.
Образование молекул АТФ, запасание энергии в удобной форме в любой клетке идет в специализированных органеллах - митохондриях (биохимики сокращают это слово до двух букв - MX), этих энергетических фабричках живого организма
Так вот, прежде полагали, что и энергия, необходимая для фотосинтеза, черпается из того же источника: из синтезируемых в MX молекул АТФ. Однако в 1954 году Арнон показал, что это не так. Хлоропласта, оказывается, полностью автономны: сами снабжают себя энергией: при освещении изолированных хлоропластов в них из АДФ и неорганического фосфата также образуется АТФ.
Этот процесс и называется фотосинтетическим фосфорилированием в отличие от окислительного фосфорилировакия, идущего в митохондриях, где молекулы АТФ образуются не под действием света, а при окислении кислородом воздуха углеводов и жиров - этих конечных продуктов фотосинтеза.
С точки зрения живой энергетики (биоэнергетики, идущей в любой клетке) АТФ - очень удобное соединение. Однако зги молекулы не могут накапливаться в клетках в очень больших количествах, так как при этом развилось бы чересчур высокое осмотическое давление. Поэтому энергия АТФ переводится в такую форму, в которой она уже может запасаться практически в любом количестве. В любом растении изготовленные светом АТФ используются для синтеза жиров и углеводов. Последние нерастворимы (не меняют осмотического давления клетки), а потому и могут откладываться про запас.
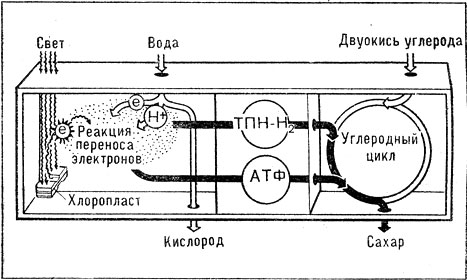
Схематическое изображение 'светлых' и 'темных' стадий в процессе фотосинтеза
Это и есть та пища (читай, энергия), которую растения изготавливают как для собственных нужд, так и на потребу всему животному миру. Склады (амбары, закрома) энергии в случае необходимости могут затем (уже в митохондриях - окислительное фосфорилирование) снова превращаться в молекулы АТФ - в нужном месте, в нужном количестве.
Еще одно существенное замечание. Выше уже упоминалось, что в большинстве европейских языков прежде вместо слова "фотосинтез" употребляли выражение "ассимиляция углекислоты". Тем самым подчеркивалось, что главное в этом процессе - это синтез углеводов и других органических продуктов. Таким образом, раньше фотосинтез ассоциировался с тем, что мы в этой главе называли словом "темное".
Сейчас взгляды начинают изменяться. Двухвековые исследования фотосинтеза (и особенно усилия ученых в последние два-три десятка лет) показывают: уникальность фотосинтеза в ином. Самое сложное (что умеют растения, но пока еще не могут люди) здесь - это процесс непосредственного преобразования солнечной энергии (квантов света) в энергию химических связей (образование АТФ в фотосинтетическом фосфорилировании и выделение из воды химически активного водорода). Самое трудное - это познать тайны светлого!
13
Красновский, родился в 1913 году, советский биохимик и био-физик, академик (1976), ученик А. Н. Теренина, окончил Московский химико-технологический институт (1937), в 1945 году Теренин вместе с Красновским (он был тогда докторантом Теренина) организует в Институте биохимии Академии наук СССР лабораторию фотобиохимии, в ней Красновский работает и до сих пор. Мысль о том, что хлорофилл способен инициировать окислительно-восстановительные реакции, впервые (1893) высказал русский ученый А. Н. Бах, но это надо было доказать прямыми и неопровержимыми экспериментами, что и сделал в 1948 году Красновский: теперь все это стало классикой, освящено известными во всем мире словами - "реакция Красновского", "красная форма Красновского". Красновский открыл существование различных форм молекуп хлорофилле (мономерные, агрегированные, комплексы с белками), им также предложен ряд моделей химической Эволюции фотосинтеза.
Москва. Ленинский проспект, 33.
Мы в Институте биохимии Академии наук СССР имени А. Н. Баха. В лаборатории фотобиохимии, которой вот уже два десятка лет руководит академик Александр Абрамович Красновский.
"Жизнь на Земле основана на фотосинтезе растений, - рассказывает Красновский. - Они, используя даровую энергию Солнца, обеспечивают животных и человека пищей и кислородом. Поглотив квант света, молекула хлорофилла запускает сложнейший механизм фотофизических, фотохимических, биохимических и иных процессов. Их расшифровкой ученые заняты вот уже 200 лет. По числу публикаций хлорофилл, вероятно, занимает первое место среди всех химических соединений, и список работ непрерывно пополняется. Занимается исследованиями хлорофилла и его аналогов и наша лаборатория..."
Во врехмя бесед с сотрудниками лаборатории Красновского и с ним самим узнал я о феофитине.
Если в молекуле хлорофилла удалить магний, то получится его безмагниевый аналог феофитин, так сказать, оправа без драгоценного камня.
При выделении хлорофилла из крапивы (стандартная процедура) феофитин получали не раз, но считали, что это лишь - результат деструкции, разрушения молекулы хлорофилла - словом, издержки производства, артефакт, как говорят люди науки. Но это было не так. И обнаружили это совсем недавно, когда вплотную занялись изучением так называемых реакционных центров, тех структурных единиц в хлоропласте, где и происходит первичное преобразование света.
"Понятно, с каким интересом и надеждой занимаются ученые исследованием этих объектов. То, что я рассказываю, - продолжает Красновский, - события последних двух-трех лет. Это еще, если можно так выразиться, совсем горячие следы науки. Работа ведется преимущественно в ряде лабораторий США и СССР: пока изучены лишь реакционные центры пурпурных бактерий.
Применяются тончайшие методы разборки биологических структур. Живая ткань растений, будто детские кубики, разбирается на отдельные блоки, подсистемы. Здесь помогают детергенты - поверхностно-активные вещества, растаскивающие, разъединяющие отдельные компоненты системы, и изощренная техника выделения частей целого.
В бактериях (в высших растениях пока, увы, нет!) удалось получить этот центр в чистом виде и проанализировать. И вот здесь исследователей ждала неожиданность: основными кирпичиками реакционных центров оказались не только молекулы хлорофилла, но и феофитина. Тот самый феофитин, который так долго третировали. Выяснилось, что система "хлорофилл - феофитин", по-видимому, является универсальным участником эстафеты переноса электрона в реакционных центрах любого фотосинтетика..."
Если здоровый, способный к фотосинтезу зеленый лист растения, лежащий на стекле, легко прокатать стеклянной палочкой, то, сохранив в себе все химические компоненты, лист все же утеряет способность к фотосинтезу.
Этот простой опыт наглядно демонстрирует важность структуры в живых тканях. Все физические и химические ингредиенты должны быть собраны, упакованы вместе в совершенно определенную целостную структуру.
Так, гем без несущего его на себе белка глобина теряет свои замечательные свойства. И хлорофилл, его дееспособность теснейшим образом связана с белковыми и иными структурами.
Головка молекулы хлорофилла гидрофильна, как и белки, она хорошо смачивается водой. А его фитольный хвост, напротив, гидрофобен - отталкивает воду, хорошо растворяясь в жирах, липидах.
Собственно, гидрофобный хвост хлорофилла и нужен ему, чтобы с его помощью внедриться, встроиться в липидную часть биологических мембран, повернув свою головку к белковым структурам.
(Если бы гем, неустанно перемещающийся по руслам кровеносных артерий, не был бы таким бродягой, а сидел на одном месте, он, вероятно, также обзавелся бы фитольным хвостом!)
Исследования фотосинтеза вступили в третью очень важную стадию.
Почти столетие после открытия Пристли ученые выясняли суть фотосинтеза; по существу, они дали определение этому процессу. Ответили на вопросы: что происходит, кто участники, что получается в итоге?
Еще примерно век ушел на то, чтобы рассмотреть детали, подробности этого уникального процесса, получить ответ на вопрос "как?". Здесь было открыто светлое и темное, прояснен их смысл.
Было сделано немало, но и число вопросов, проблем за это время также неизмеримо возросло. Эту жажду новых знаний подхлестывает появление новой сверхчувствительной экспериментальной техники.
И сейчас исследователи уже жаждут ответов на вопрос "почему?". Начинается третий, решающий этап изучения фотосинтеза.
Структура - вот пароль новейших исследований.
Изучить хлорофилл и феофитин, действующие не в искусственно приготовленных растворах (хотя бы и хитро подобранных), а в живых белково-липидных комплексах на биологических мембранах. Это и есть высший и наиболее трудный этап в изучении пигментов растений (если говорить о них).
Да, задача не из легких.
Если, скажем, заняться механизмом функционирования реакционного центра фотосинтезирующих бактерий, то выяснится, что согласно новейшим данным: в него входят 3 субъединицы белка (громадные в сравнении с пигментами образования), 4 молекулы (агрегированные в димеры) бактериохлорофилла (хлорофиллы бактерий и растений несколько отличаются), 2 молекулы бактерио-феофитина, 1-2 атома железа в комплексе с убихиноном. И все это вмонтировано в мембраны, сопряжено между собой тончайшими связями.
Вот какой сложный объект (в действии!) предстоит познать ученым. И хотя они вооружены самой новейшей аппаратурой - лазерами, импульсными спектрофотометрами и другими могучими приборами, работа предстоит им нелегкая.
Структурные исследования не только ответят на вопрос "почему?", но и позволят в будущем сконструировать искусственные фотосинтетические системы, не просто повторяющие то, что создано Природой, а превосходящие его.
|
|
© PLANTLIFE.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://plantlife.ru/ 'PlantLife.ru: Статьи и книги о растениях'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://plantlife.ru/ 'PlantLife.ru: Статьи и книги о растениях'