
Биохимия фотосинтеза
Лучше всего познакомиться с процессом фотосинтеза можно, вероятно, рассмотрев четыре главных вопроса: 1) каким образом поглощается световая энергия? 2) каким, образом она переводится в форму, пригодную для выполнения химической работы? 3) какая последовательность реакций приводит к высвобождению кислорода из молекул воды? 4) какой путь ведет к превращению двуокиси углерода в сахар? Каждый из этих вопросов в отдельности мы теперь и обсудим.
Поглощение лучистой энергии
Свет может вызвать фотохимический эффект лишь после того, как он будет поглощен. Вещества, поглощающие видимый свет, называются пигментами. Поглощение пигментом кванта света (фотона) определяется характером распределения электронов в молекуле данного пигмента; какие именно длины волн будет поглощать пигмент, зависит от числа и от расположения двойных связей в его молекуле, а также от присутствия в ней ароматических колец. В результате поглощения фотона пигментом распределение электронов в его молекуле несколько изменяется и пигмент переходит в иную, "активированную", форму. Поскольку между длиной волны поглощаемого света и структурой поглощающего вещества существует определенная связь, мы можем установить характеристики пигмента, играющего роль фоторецептора в определенной фотохимической реакции, по данным, показывающим, как изменяется его активность в зависимости от длины волны.
Направляя на зеленый лист монохроматический свет различной длины волны, полученный с помощью светофильтра, призмы или дифракционной решетки, и измеряя скорость фотосинтеза, соответствующую каждой длине волны, можно убедиться в том, что свет в синей (~420 нм) и красной (~670 нм) областях спектра обеспечивает наибольшую эффективность фотосинтеза, а свет в зеленой (~500-600 нм) области - наименьшую (рис. 4.7). Такой спектр действия (зависимость относительной эффективности процесса от длины волны) можно объяснить, исходя из спектра поглощения хлорофилла, главного пигмента хлоропластов. Экстрагированный из листьев хлорофилл интенсивно поглощает как раз в тех диапазонах длин волн, которые наиболее эффективны в фотосинтезе (рис. 4.8). Само это сходство между "спектром поглощения" хлорофилла и "спектром действия" фотосинтеза является одним из лучших доказательств того, что роль главного рецепторного пигмента в фотосинтезе играет именно хлорофилл. Отдельные особенности спектра действия фотосинтеза указывают, что в поглощении света при этом процессе участвуют также и желтые пигменты - каротиноцды, которые наряду с хлорофиллом в большом количестве содержатся в хлоропластах. В отсутствие хлорофилла каротиноиды неспособны осуществлять фотосинтез, поэтому принято считать, что активированные светом каротиноиды передают поглощенную ими энергию хлорофиллу, который в конечном счете и выполняет собственно фотосинтетическую работу.
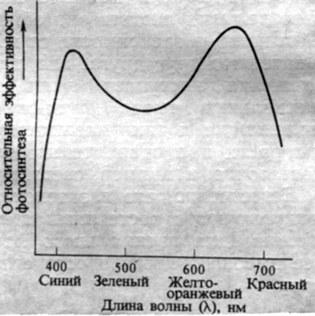
Рис. 4.7. Спектр действия фотосинтеза для зеленого листа
Расчеты показывают, что в перенос электронов при фотосинтезе в действительности вовлекается только небольшая часть молекул хлорофилла. Прочие его молекулы выполняют лишь роль светособирающего комплекса, или светособирающей антенны. Передача энергии от каротиноидов к хлорофиллу и от одной молекулы хлорофилла к другой происходит в результате процесса, который называют резонансным переносом. Участвующие в этом процессе молекулы должны быть плотно упакованы, для того чтобы колебательная энергия могла непосредственно передаваться от одной молекулы к другой. В гранах хлоропластов у высших растений фотосинтетические пигменты именно так и упакованы, о чем мы уже говорили в гл. 2; поэтому энергия, поглощенная одним из пигментов, легко может быть передана молекулам некоторых других пигментов.
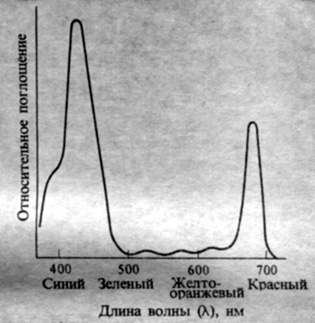
Рис. 4.8. Спектр поглощения хлорофилла a в эфире
У пурпурных фотосинтезирующих бактерий имеется пигмент бактериохлорофилл - структурный аналог хлорофилла. Этот пигмент поглощает в зеленом и инфракрасном участках спектра, т. е. в тех областях, где высшим зеленым растениям интенсивное поглощение не свойственно. Красные, бурые и сине-зеленые водоросли содержат наряду с хлорофиллом также и большие количества пигментов из группы фикобилинов (фикоэритрин, фикоцианин, аллофикоцианин и другие, родственные желчным пигментам животных); кроме того, в них присутствуют и каротиноиды, такие, как фукоксантин и перидинин. Перечисленные пигменты образуют ассоциации, которые у этих водорослей играют роль главной светопоглощающей системы. Фикоэритрин поглощает в сине-зеленой области спектра и потому кажется красным, тогда как фикоцианин и аллофикоцианин наиболее интенсивно поглощают в желтом и красном диапазонах и соответственно окрашены в синий или зеленый цвет (рис. 4.9). Спектр действия фотосинтеза у этих водорослей (рис. 4.10) заметно отличается от спектра зеленых растений.
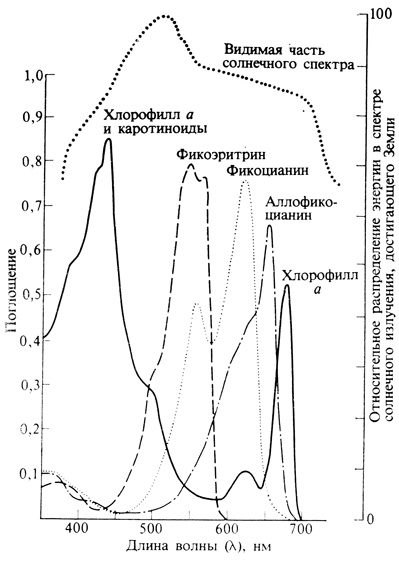
Рис. 4.9. Спектры поглощения пигментов, экстрагированных из сине-зеленых водорослей. (Е. Gantt. 1975. BioScience, 25, 781-788.) У хлорофилла а (сплошная линия) главные максимумы поглощения лежат при 435 и 675 нм. Поглощение фикобилинов (фикоэритрина, R-фикоцианина и аллофикоцианина), выделенных в виде фикобилинпротеидов из фикобилисом, хорошо заполняет разрыв в той области, где хлорофилл поглощает очень слабо. Спектры флуоресценции этих пигментов достаточно хорошо перекрываются, что создает целостную систему переноса энергии. В верхней части рисунка показано распределение энергии в видимой части солнечного спектра
Пигменты водорослей, присоединенные к белкам, сгруппированы в структурные единицы, фикобилисомы, располагающиеся в хлоропластах на той стороне ламелл, которая обращена к строме. Все пигменты флуоресцируют, т. е. каждый из них поглощает фотоны определенной энергии и определенной длины волны и испускает фотоны меньшей энергии с несколько большей длиной волны. Таким образом, в результате ряда актов поглощения и испускания света световая энергия в конечном счете передается хлорофиллу.
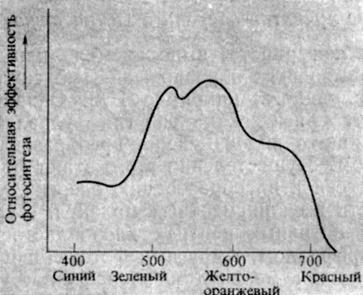
Рис. 4.10. Спектр действия фотосинтеза у красной водоросли Porphyra. (F. T. Haxo, L. R. Blinks. 1950. J. Gen. Physiol., 33, 389-422.)
Фикобилины, на долю которых приходится у некоторых водорослей до 60% всего белка, образуют достаточно эффективную светособирающую систему, хотя передача энергии между этими пигментами происходит все же не столь эффективно, как в хлоропластах высших растений. Есть водоросли, у которых соотношение различных фикобилинов меняется в зависимости от спектрального состава света. Такие водоросли при освещении светом разных длин волн меняют свою окраску. Это явление получило название хроматической адаптации. Если, например, выращивать такие водоросли на красном свету, то у них будет преобладать фикоцианин, если же освещать их зеленым светом, то главное место займет фикоэритрин. Подобная приспособляемость позволяет водорослям, растущим на разной глубине, поглощать достаточно света, необходимого для фотосинтеза, хотя свет с увеличением глубины меняет свой спектральный состав, так как часть его энергии при прохождении через слой воды поглощается или же рассеивается молекулами воды или взвешенными в воде частицами. Не все водоросли обладают способностью к хроматической адаптации. Некоторые из них выживают на разной глубине благодаря тому, что с увеличением глубины они синтезируют больше пигмента.
Преобразование лучистой энергии в химическую
Фотохимическая работа, выполняемая при фотосинтезе, в конечном счете сводится к разложению молекул воды или какого-нибудь ее аналога, например H2S. Однако, прежде чем это произойдет, "физическая" энергия уловленных фотонов должна быть как-то видоизменена, преобразована в "химическую" энергию. В осуществлении этого этапа фотосинтеза, т. е. этапа, сводящегося к преобразованию энергии, участвует лишь небольшая часть всех пигментных молекул, сосредоточенная в фотохимически активных центрах хлоропластов. Энергия, поглощенная хлорофиллом и другими фотоактивированными пигментами, передается молекулам хлорофилла, находящимся в этих фотохимически активных центрах, или ловушках. В результате отдельным электронам сообщается достаточное количество энергии для того, чтобы они могли перейти от молекул хлорофилла в фотохимически активных центрах к другим, находящимся поблизости молекулам, к так называемым переносчикам электронов. Переносчик поглощает определенную часть этой энергии активации и передает электрон следующему переносчику, где тот же процесс повторяется. В хлоропластах различные переносчики электронов размещены на мембране или внутри мембраны и образуют здесь некий ряд, в пределах которого они располагаются в соответствии с их способностью присоединять электроны (иными словами, с их "окислительно-восстановительным потенциалом"). Таким образом, электрон переходит от одного переносчика к другому, подобно тому как низвергается по каскаду вода - с одного уступа на другой. Во время перемещения электрона по такой цепи переносчиков часть его энергии переводится в химическую форму, поскольку за счет этой энергии из аденозиндифосфата (ADP) и неорганического oфосфата (Pi) синтезируется аденозинтрифосфат (ATP) (рис. 4.11). В химической связи между ADP и Pi запасается значительное количество энергии (8-10 ккал/моль) и эта энергия высвобождается в процессе реакций, в которых указанная связь разрывается. Синтез АТР, протекающий с использованием энергии видимой части солнечной радиации, носит название фотофосфорилирования. ATP - это "энергетическая валюта" живых клеток. Многие реакции, идущие в клетке с потреблением энергии (эндергонические реакции), получают эту энергию именно в результате распада ATP до ADP и либо Pi либо какого-нибудь другого фосфорилированного соединения.
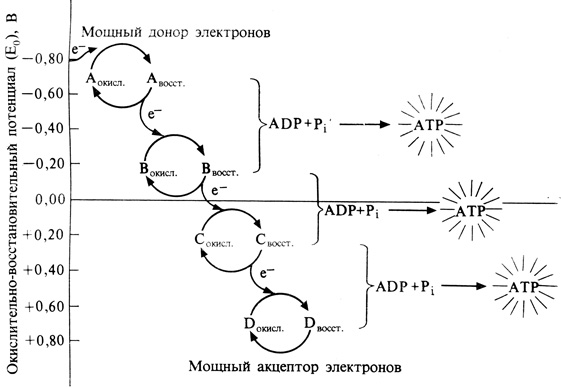
Рис. 4.11. A, B, C и D - переносчики электронов, расположенные в порядке убывания их окислительно-восстановительного потенциала (который становится при этом менее отрицательным). Разность потенциалов между двумя соседними переносчиками, превышающая 0,16 В, достаточна для присоединения Pi к ADP, т. е. для синтеза ATP
Более 20 лет назад Роберт Эмерсон обнаружил, что красный свет с длиной волны более 700 нм, относительно малоэффективный в фотосинтезе высших растений, становится вполне эффективным, если использовать его совместно с более коротковолновым красным светом. Это явление, названное "эффектом усиления Эмерсона", было положено в основу гипотезы, согласно которой фотосинтез включает две разные световые реакции и оптимальные условия создаются для него в том случае, когда две эти реакции протекают одновременно. Гипотезу подкрепило выделение из хлоропластов высших растений двух отдельных систем, получивших названия фотосистема I и фотосистема II (рис. 4.12). Каждая из этих фотосистем характеризуется своим особым набором молекул хлорофилла и связанных с ними переносчиков электронов и каждая осуществляет свои, присущие только ей фотосинтетические реакции. Фотосистема I - единственная, имеющаяся у бактерий - работает без участия кислорода, поскольку бактерии - это самые примитивные автотрофы; фотосистема I, по-видимому, преобладала на ранних этапах биологической эволюции, когда кислорода в земной атмосфере было мало. С развитием фотосистемы II растения получили возможность выделять молекулярный кислород из воды. Именно это обстоятельство, очевидно, и определило изменение свойств земной атмосферы: из анаэробной она стала теперь аэробной.
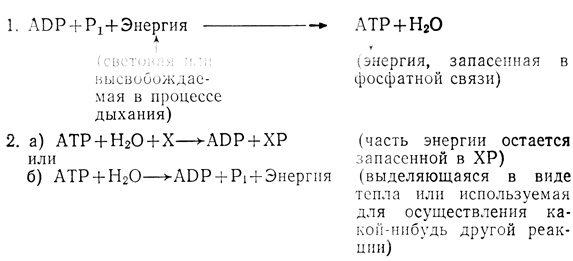
Хлорофилл, являющийся энергетической ловушкой фотосистемы I, обозначают символом P700, поскольку максимум поглощения приходится у него на 700 нм. При поглощении кванта света один из электронов P700 переходит на более высокий энергетический уровень. В этом состоянии он захватывается белком? содержащим железо и серу (FeS), а затем передается переносчику, который называется ферредоксином. Далее электрон следует по одному из двух возможных путей. Один путь (циклическое фотофосфорилирование) состоит из поэтапного переноса электрона от ферредоксина обратно к P700 через ряд промежуточных переносчиков, среди которых имеются флавопротеиды, содержащие витамин B2, и гемсодержащие цитохромы. В то время как электрон перемещается по этому циклическому пути, энергия его используется для присоединения Pi к ADP с образованием ATP. Кислород в циклическом фотофосфорилировании не участвует, и поскольку газообмена между внутренним пространством листа и атмосферой не происходит, теоретически фотосинтез такого типа может протекать и при закрытых устьицах. Циклическое фотофосфорилирование - единственный функциональный путь фотосинтеза в монохроматическом свете с длиной волны более 700 нм, потому что для активации фотосистемы II необходимо более коротковолновое излучение. Однако нам пока еще трудно судить о том, насколько важную роль играет циклическое фотофосфорилирование в листьях.
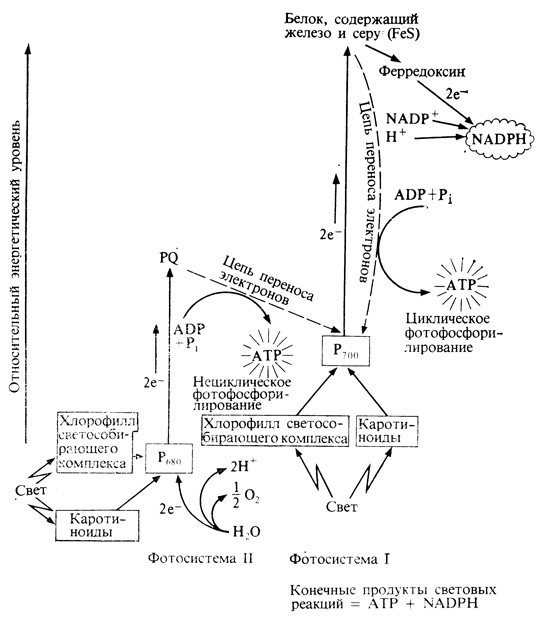
Рис. 4.12. Z-схема световых реакций фотосинтеза
Нециклическое фотофосфорилирование и выделение кислорода
Когда устьица листа открыты, а хлоропласты поглощают смешанный свет разных длин волн, одновременно с фотосистемой I включается и фотосистема II. В сочетании друг с другом они составляют систему нециклического фотофосфорилирования. В этих условиях активированные электроны, отданные P700, переносятся сначала на FeS, а затем на ферредоксин. В этой точке они отклоняются от циклического пути и переносятся - через различные флавопротеиды - на NADP+, ниацинсодержащее соединение, восстановленная форма которого (NADPH) используется в последующих реакциях для восстановления CO2 до уровня углевода. Теперь хлорофилл энергетической ловушки фотосистемы II, P6SO, также переходит в возбужденное состояние и отдает электрон. Пройдя через ряд переносчиков (пласто- хинон, цитохром f, пластоцианин), этот электрон в конце концов достигает P700 и заполняет здесь "дырку", возникшую, когда эта система, перейдя в возбужденное состояние в результате поглощения света, потеряла электрон. P680, входящий в фотосистему II, в свою очередь заполняет образовавшуюся в нем дырку, присоединяя электрон от иона OH-, продукта ионизации воды. По-видимому, два возникших таким путем "свободных радикала" (2OH•) объединяются и образуют перекись, которая в конце концов распадается, что и приводит к выделению кислорода. Для этой реакции выделения кислорода необходимы в качестве кофакторов ионы марганца и хлора, а ингибитором ее может служить синтетический гербицид диурон (дихлорфенилдиметилмочевина). Растения, обработанные диуроном, гибнут, вероятно, в результате накопления перекиси или каких-нибудь других высокоокисленных соединений. Кроме того, при этом блокируется перенос электронов от воды, не образуется ATP и не восстанавливается NADP+. Диурон, следовательно, токсичен лишь для зеленых растений на свету; для прочих же организмов, в том числе и для человека, он, по-видимому, безвреден.
При ионизации воды образуются еще и ионы H+. Они остаются в водной среде тилакоидов хлоропластов, состоящей, как мы помним, не только из молекул воды, но также из H+- и OH-- ионов. Однако накопление H+-ионов на внутренней стороне мембраны тилакоидов играет определенную роль в образовании ATP (см. ниже). По фотосистемам передаются лишь отданные хлорофиллом электроны, хотя протоны (H+-ионы) проходят вместе с электронами часть пути по цепи переносчиков. Когда два электрона присоединяются в конечном счете к NADP+, из водной среды, окружающей тилакоидные мембраны, извлекаются свободные протоны и таким путем образуется NADPH. Весь этот процесс, представленный на рис. 4.12, получил название "Z-схемы".
Как образуется ATP
Мы в своем изложении исходили из того, что основой синтеза ATP является перенос электронов. В последнее время, однако, широкое признание получила хемиосмотическая теория английского исследователя Питера Митчелла, в основу которой положено представление о перемещении протонов.
Рассмотрим синтез ATP в хлоропластах (рис. 4.13), где легко проследить его связь с "Z-схемой" световых реакций фотосинтеза (рис. 4.12). Фотосинтетическая цепь переноса электронов размещается в тилакоидной мембране. Один из находящихся здесь переносчиков электронов, пластохинон, переносит наряду с электронами и протоны (H+-ионы), перемещая их через тилакоидную мембрану в направлении снаружи внутрь. Следствием этого является повышение концентрации протонов внутри тилакоида и возникновение значительного градиента pH между наружной и внутренней стороной тилакоидной мембраны: с внутренней стороны среда оказывается более кислой, чем с наружной. Эта повышенная кислотность внутри тилакоида еще более усиливается вследствие фотолиза, при котором электроны и O2 удаляются, а протоны накапливаются. Значительный градиент pH между внутренней и наружной стороной тилакоидной мембраны представляет собой потенциальный источник энергии. Эта энергия может использоваться при обратном перемещении протонов изнутри наружу по особым каналам в "грибовидных выростах", находящихся на наружной стороне тилакоидной мембраны. В каналах находится белок, так называемый фактор сопряжения (ФС1), способный осуществлять синтез ATP. Этот белок, вообще говоря, представляет собой ATP-азу, т. е. фермент, катализирующий распад ATP, но при наличии соответствующей энергии он может катализировать и синтез данного соединения. Энергию поставляют протоны, текущие сквозь мембрану, через ножки и головки грибовидных выростов. Все в целом напоминает преобразование механической энергии в электрическую в гидротурбине. Протоны текут по каналам в грибовидных выростах до тех пор, пока их концентрация внутри тилакоида превышает наружную концентрацию и, значит, пока электроны под воздействием поглощаемого хлорофиллом света перемещаются по цепи переносчиков. На каждые два переданных по цепи электрона внутри тилакоида накапливается приблизительно четыре протона. На каждые три протона, возвращающиеся (с участием фактора сопряжения) обратно наружу" синтезируется одна молекула ATP.
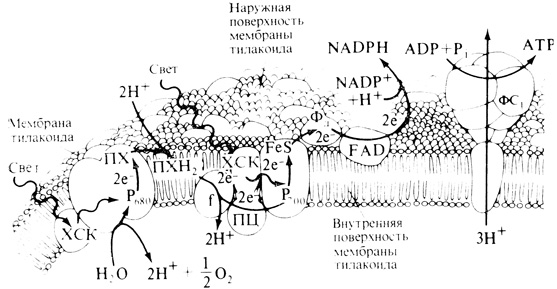
Рис. 4.13. Схематическое изображение цепи переноса электронов, поясняющее, каким образом эта система транспортирует через мембрану тилакоида протоны и осуществляет синтез ATP. (С любезного разрешения R. E. McCarty, P. С. Hinkle, Cornell University. Рисунок M. Hinkle.) Лучистая энергия, поглощенная хлорофиллом, выполняющим роль светособирающего комплекса (ХСК), передается P680 и P700, способным также поглощать свет непосредственно. От возбужденных молекул P680 и P700 отрываются пары электронов, в результате чего в молекулах остаются участки с избыточным положительным зарядом, называемые дырками. Электроны от P680 улавливаются особой формой переносчика электронов, пластохиноном (ПХ). В этой точке за электронами следуют два протона из стромы, находящейся кнаружи от тилакоида, так что пластохинон восстанавливается в ПХН2. Эти протоны затем освобождаются, поступая внутрь тилакоида, а электроны передаются сначала цитохрому f(f), затем пластоцианину (ПЦ) и, наконец, P700, где они заполняют дырку. Электроны от P700 улавливаются белком, содержащим железо и серу (FeS), после чего передаются ферредоксину (Фд), флавинадениндинуклеотиду (FAD) и, наконец, NADP+. Протон, поступивший в тилакоид снаружи, присоединяется к двум электронам и NADP+ с образованием NADPH. Цикл завершается после того, как H2O внутри тилакоида претерпевает фотолиз, дающий 2 электрона, 2 протона и 1/2 O2. Электроны заполняют дырку в молекуле P680, кислород выделяется в газообразной форме, а протоны, находившиеся внутри тилакоида, перемещаются обратно, наружу, через фактор сопряжения (ФС1 на схеме справа). Энергия, высвобождающаяся при этом перемещении протонов, используется для синтеза ATP из ADP и Pi
Восстановление CO2 до углевода
Конечными продуктами световых реакций фотосинтеза являются NADPH и ATP (рис. 4.14). Эти соединения используются затем соответственно как восстановительная сила и как источник энергии для превращения CO2 в сахар. Этапы, из которых слагается это превращение, известны под общим названием "темповых реакций" фотосинтеза.
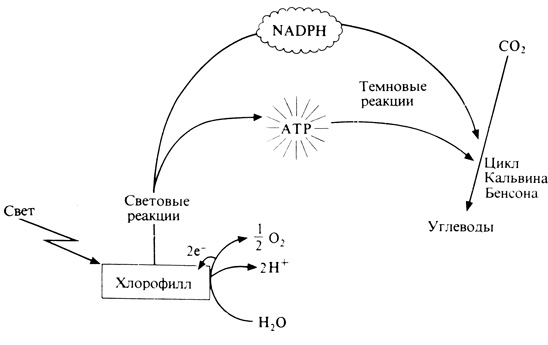
Рис. 4.14. Продукты световых и темновых реакций фотосинтеза
Последовательность реакций на пути превращения CO2 в сахар удалось выяснить благодаря применению радиоактивного углерода, 14C. Этот изотоп углерода, распадающийся с испусканием p-частиц, можно обнаружить при помощи счетчика Гейгера-Мюллера или любого другого детектора радиоактивных излучений. Вводя в фотосинтезирующие клетки радиоактивную CO2, а затем отбирая через определенные промежутки времени различные химические фракции и измеряя их радиоактивность, можно проследить биохимический путь, который проходит в этих клетках 14C. Мелвин Кальвин и Эндрью Бенсон из Калифорнийского университета в Беркли воспользовались этим методом для того, чтобы установить путь фиксации углерода у одноклеточной зеленой водоросли Chlorella. Фотосинтез в клетках Chlorella происходил в присутствии радиоактивной CO2. Образующиеся меченые соединения экстрагировали из клеток метанолом, после чего исследуемую смесь разделяли на отдельные компоненты методом двумерной хроматографии на бумаге. Согласно этому методу, разделение смеси проводят сперва в одном направлении с помощью одной системы растворителей, а затем под прямым углом к первому направлению используют другую систему растворителей. На полученную хроматограмму накладывали рентгеновскую пленку. После проявления этой пленки темные пятна обнаруживались на ней во всех тех местах, где находились соединения, содержавшие радиоактивный углерод. Таким способом удалось выяснить, что в процессе фотосинтеза за несколько минут образуется большое число меченых соединений. Однако, когда время, отведенное на фотосинтез, сократили до 0,5 с, обнаружить удалось одно только трехуглеродное фосфорилированное соединение - 3-фосфоглицериновую кислоту (ФГК). Отсюда был сделан вывод, что ФГК - это первый стабильный продукт, образующийся из CO2 в процессе фотосинтеза.
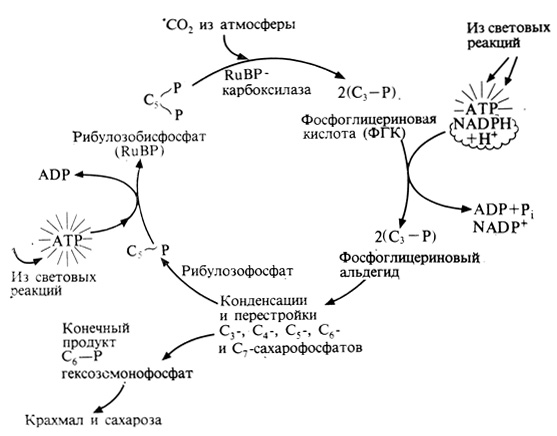
Рис. 4.15. Упрощенная схема цикла Кальвина-Бенсона для темновых реакций фотосинтеза
Ступенчатая деградация выделенной радиоактивной ФГК дает возможность показать, что радиоактивную метку (ее обозначают символом *C или 14C) несет карбоксильная (COOH) группа ФГК и что, следовательно, именно она представляет собой видоизмененную форму исходной 14CO2. Можно было бы предположить, что поглощаемая 14CO2 соединяется с каким-то двууглеродным фрагментом, в результате чего и образуется ФГК, но это не подтвердилось. Кальвин и Бенсон занялись поисками соединения, которое накапливалось бы после исчерпания запаса 14CO2 в процессе фотосинтеза. Они исходили из предположения, что накапливаться в этих условиях должен был как раз неиспользованный "акцептор CO2". Такое соединение действительно было найдено (рис. 4.15 и 4.16) и было идентифицировано как рибулозобисфосфат (RuBP) - пятиуглеродное фосфорилированное соединение, распадающееся после присоединения CO2 на две молекулы ФГК. Фермент, катализирующий эту реакцию, рибулозобисфосфат-карбоксилаза, занимает в количественном отношении первое место среди белков, содержащихся в зеленой ткани.
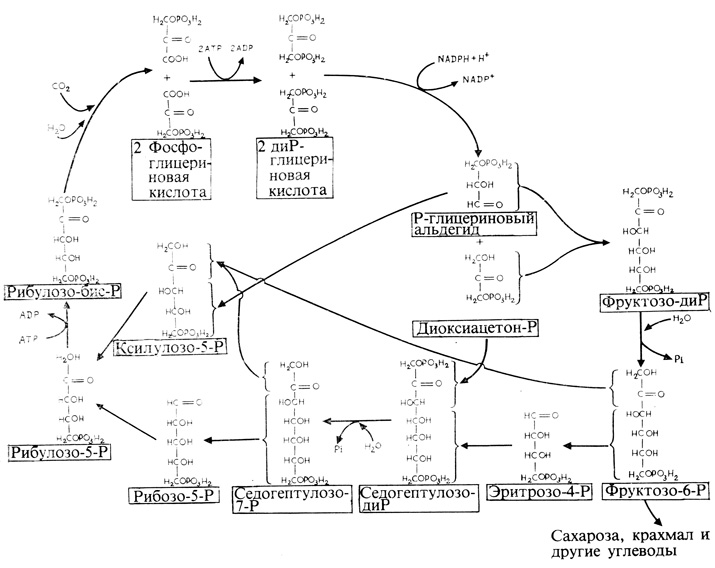
Рис. 4.16. Более подробное изображение цикла Кальвина-Бенсона. P везде
Фосфоглицериновая кислота, образующаяся из CO2, еще не достигает уровня восстановленности углеводов, который соответствует альдегидной группе (H-C=O); она отстоит от него на одну ступень, т. е. степень ее окисления соответствует карбоксильной группе (HO-C=O). Восстановление до уровня альдегида осуществляется за счет восстановительной силы NADPH и энергии ATP - двух соединений, представляющих собой продукты световых реакций фотосинтеза. Этот последний этап обпязования сахара из CO2 через ФГК может быть схематически изображен в следующем виде:
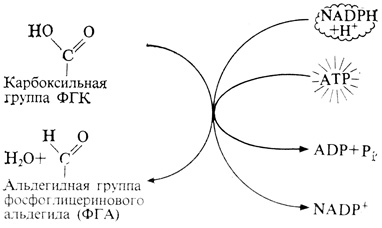
Фосфоглицериновый альдегид, представляющий собой фосфорилированное производное сахара, содержит только три атома углерода. Между тем в простейшем сахаре, который накапливается в растениях в сколько-нибудь значительном количестве, содержится шесть атомов углерода. Для того чтобы образовалась гексоза, две молекулы фосфоглицеринового альдегида (или каких-либо простых его производных) должны соединиться "голова к голове" и продукт этого присоединения, гексозобис-фосфат, должен подвергнуться дефосфорилированию.
После этого гексоза из цикла может направляться либо на синтез сахарозы и полисахаридов, либо - через дыхательный путь (см. гл. 5) - на построение углеродных скелетов любых других органических соединений клетки. Таким образом, сахар, образующийся в процессе фотосинтеза из CO2, - это основное органическое вещество, которое в клетках высших растений служит источником как энергии, так и необходимых клетке строительных блоков.
|
|
© PLANTLIFE.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://plantlife.ru/ 'PlantLife.ru: Статьи и книги о растениях'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://plantlife.ru/ 'PlantLife.ru: Статьи и книги о растениях'