
Способы питания водорослей и других хлорофиллоносных растений (В. Е. Семененко)
Несмотря на удивительное многообразие жизненных форм растений, подавляющее большинство из них объединяет уникальная особенность, которая определяется способом их питания. В отличие от животных организмов и многих бактерий, использующих для своей жизнедеятельности готовые органические соединения, у растений выработалась в ходе эволюции способность использовать для питания такие полностью окисленные вещества, как углекислота и вода, и создавать на их основе органические соединения. Процесс этот осуществляется в природе за счет энергии солнечного света и сопровождается выделением кислорода. Использование световой энергии для биологических синтезов стало возможно благодаря появлению у растений комплекса поглощающих свет пигментов, главнейшим из которых является хлорофилл. Процесс светового и углеродного питания растений получил название фотосинтеза и в общем виде может быть записан следующим суммарным уравнением:
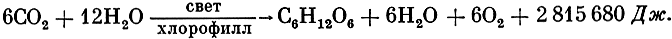
Из уравнения видно, что на каждые 6 грамм- молекул углекислоты и воды синтезируется грамм-молекула глюкозы (С6Н12О6), выделяется 6 грамм-молекул кислорода и накапливается 2 815 680 Дж энергии. Таким образом, функция фотосинтеза растений является, по существу, биохимическим процессом преобразования световой энергии в химическую.
Водоросли, уже простейшие из них - сине-зеленые, являются первыми организмами, у которых появилась в процессе эволюции способность осуществлять фотосинтез с использованием воды в качестве источника (донора) водорода и выделением свободного кислорода, т. е. процесс, свойственный всем другим водорослям, а за ними и высшим растениям.
Осуществляемый растениями в грандиозных масштабах процесс преобразования энергии света в химическую энергию продуктов фотосинтеза является практически единственным "руслом", через которое "вливается" в биологически приемлемой форме энергия, необходимая для поддержания жизни и круговорота веществ в биосфере нашей планеты. Именно поэтому выдающийся русский естествоиспытатель К. А. Тимирязев говорил о "космической роли зеленых растений". О размерах фотосинтетической деятельности растений в планетарном масштабе можно судить по тому, что весь кислород атмосферы Земли имеет, как сейчас доказано, фотосинтетическое происхождение. Залежи каменного угля представляют собой своеобразный "запас" некогда преобразованной в результате фотосинтеза растений солнечной энергии, складированный в определенные геологические эпохи.
Второй особенностью питания водорослей и других фотосинтезирующих растений, не менее важной, хотя и не такой специфичной, как фотосинтез, является их способность усваивать азот, серу, фосфор, калий и другие минеральные элементы в виде ионов минеральных солей (NО3-, SО4--, РО4---, К+ и др.) и использовать их для синтеза таких важнейших компонентов живой клетки, как аминокислоты, белки, нуклеиновые кислоты, макроэргические соединения, вещества вторичного обмена (алкалоиды, терпены, фенольные соединения, различные витамины, фитогормоны и др.). Среди сине-зеленых водорослей имеются формы, способные осуществлять процесс фиксации свободного азота атмосферы и превращать его в органические азотистые вещества своего тела.
Происхождение и эволюция фотосинтеза
Каким же образом возник процесс фотосинтеза? Что ему предшествовало и к каким последствиям привело появление этого процесса на Земле?
Согласно общепризнанной в настоящее время эволюционной теории происхождения и развития жизни, которая более 50 лет назад была сформулирована А. И. Опариным, первичные, способные к самовоспроизводству живые образования возникли в результате абиогенной химической эволюции. Будучи окруженными близкими по составу, но еще неживыми органическими соединениями, эти первичные существа могли осуществлять в бескислородной среде анаэробный гетеротрофный тип питания с помощью небольшого набора ферментов. Постепенное истощение и деградация органических веществ, синтезированных абиогенным путем, сопровождались накоплением все более окисленных соединений, вплоть до появления наиболее бедного энергией соединения углерода - углекислоты. Это влекло за собой необходимость все большего и большего совершенствования и усложнения ферментативного аппарата, необходимого для ассимиляции все более окисленных веществ. В этих условиях, которые все еще характеризовались отсутствием в среде кислорода, вполне вероятно возникновение первичных автотрофных организмов, которые осуществляли восстановление углекислоты за счет химической энергии, полученной из минеральных веществ. Такой тип питания получил название хеморедукции. Среди современных организмов известна группа сульфатредуцирующих микроорганизмов, которые восстанавливают сульфаты до сероводорода, используя для этой цели молекулярный водород.
Появление в этот период, который характеризовался сильно восстановительными условиями среды, светпоглощающих пигментов-фотосенсибилизаторов привело, очевидно, к замене химической энергии в процессах хеморедукции на световую. Возник простейший тип фотоавтотрофного питания, который получил название фоторедукции и бактериального фотосинтеза. Такой тип питания осуществляют современные фототрофные бактерии - пурпурные серобактерии (Thiorhodaceae) и зеленые серобактерии (Chlorobacteriaceae), у которых роль пигмента-фотосенсибилизатора выполняет бактериохлорофилл и которые являются строгими анаэробами. Пурпурные и зеленые серобактерии восстанавливают углекислоту за счет энергии света, используя в качестве Н-донора сероводород (H2S):
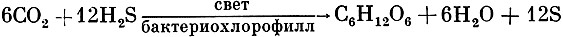
Представленное итоговое уравнение бактериального фотосинтеза (фоторедукции) очень напоминает, как мы видим, приведенное выше суммарное уравнение фотосинтеза хлорофиллоносных растений. В результате сравнительного анализа Ван-Ниль показал, что оба эти процесса могут быть записаны в общем виде одним итоговым уравнением:
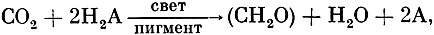
где Н2А - донор водорода, в качестве которого фотосинтезирующие бактерии используют сероводород, а остальные растения - воду. Вода является более окисленным соединением по сравнению с сероводородом. Использование ее в качестве донора водорода связано с необходимостью дополнительной затраты энергии и стало возможно благодаря дальнейшему совершенствованию фотохимического аппарата, которое состояло в появлении у растений (начиная с сине-зеленых водорослей) хлорофилла (вместо бактериохлорофилла) и дополнительной фотохимической системы, так называемой "фотосистемы П".
Использование воды в качества донора водорода привело к тому, что в процессе фотосинтеза стал выделяться кислород, что, в свою очередь, ознаменовало переход от анаэробной к аэробной жизни на нашей планете.
На эволюционную связь фоторедукции и фотосинтеза может указывать способность ряда сине-зеленых, зеленых, красных и бурых водорослей обратимо переходить к фоторедукции при переводе их в анаэробные условия в атмосферу водорода.
Таким образом, фотоавтотрофный тип питания и фотосинтез возникли в процессе эволюции как "надстройка" над первичным гетеротрофным типом питания. Появление на Земле фотосинтеза было обусловлено всем ходом предшествовавшей биологической эволюции и явилось поворотным пунктом в переходе от анаэробного к аэробному типу обмена веществ.
Рассмотренная схема дает представление лишь об общих чертах эволюции фотосинтеза и является в значительной степени гипотетической. Многие этапы эволюции фотосинтеза и тем более ее детали остаются неясными, ряд моментов по-разному интерпретируется учеными.
Неясным, например, остается вопрос о происхождении хлоропластов высших растений. Существует точка зрения об эндосимбиотическом их происхождении в результате "захвата" первичных фотосинтезирующих организмов, типа современных сине-зеленых водорослей, гетеротрофным организмом. На такую возможность указывает определенная генетическая автономность хлоропластов, а также подобие их ДНК, ряда важнейших ферментов, свойств рибосом и ряда РНК таковым у прокариотических организмов, в частности сине-зеленых водорослей. Вместе с тем имеется и определенная генетическая подчиненность хлоропласта ядерному геному, что может указывать на "прямую" эволюцию фотосинтетического аппарата современных растений от первичных фотосинтезирующих организмов. Все эти вопросы требуют дальнейшего детального изучения механизмов, молекулярной организации, генетического контроля и физиологических свойств фотосинтеза и его аппарата.
Строение и молекулярная организация фотосинтетического аппарата
Фотосинтетический процесс преобразования световой энергии протекает в клетках растений в специализированных мембранных структурах. У высших растений и эукариотических водорослей эти мембранные структуры локализованы в особых органеллах - хлоропластах. У прокариотических сине-зеленых водорослей они располагаются непосредственно в цитоплазме.
Мембраны фотосинтетического аппарата имеют общий с другими биологическими мембранами принцип строения и состоят из липидов и белков. Отличительной особенностью этих мембран является то, что в них "встроены" молекулы хлорофилла и других сопровождающих пигментов, которые поглощают свет и обеспечивают передачу энергии электронного возбуждения "активному центру" и в фотосинтетическую цепь переноса электрона.
Изучение хлоропластов с помощью электронного микроскопа показало, что мембранная система имеет здесь дифференцированную, очень сложную, но четко упорядоченную структуру, которая различается у разных растений характером упаковки и степенью ее выраженности. Мембранная система погружена в строму (или матрикс) хлоропласта, в которой локализованы ферменты, связанные с восстановлением углекислоты и синтезом углеводов. Существенным обстоятельством является то, что в хлоропластах, кроме систем, непосредственно участвующих в осуществлении процесса фотосинтеза, имеется также собственная (отличная от ядерной) ДНК, рибосомы и другие компоненты белоксинтезирующих систем. Для хлоропластов многих водорослей характерно также наличие специфического образования - пиреноида, функциональная роль которого остается неясной. Хлоропласты способны к делению и имеют чрезвычайно разнообразную форму у разных водорослей.
Пигменты фотосинтетического аппарата
Способность растений осуществлять фотосинтез связана с наличием у них пигментов. Главнейшим из них является магнийсодержащий порфириновый пигмент - хлорофилл.
В природе встречается пять разных типов хлорофилла, которые незначительно различаются по своей молекулярной структуре. Хлорофилл а присутствует у всех водорослей и высших растений; хлорофилл b - у зеленых, харовых и эвгленовых и у высших растений; хлорофилл с - у бурых водорослей, золотистых, диатомей и динофлагеллат; хлорофилл d - у красных водорослей; хлорофилл е обнаружен лишь однажды, по-видимому, это хлорофилл с; наконец, различные виды бактериохлорофилла - у фотосинтезирующих бактерий. Для сине-зеленых и красных водорослей характерно наличие билипротеинов: фикоцианина и фикоэритрина. Наиболее хорошо изучен хлорофилл а. Молекула его состоит из четырех пиррольных колец, с азотом которых связан атом магния, а к одному из колец присоединен одноатомный ненасыщенный спирт фитол.
Молекула хлорофилла встроена в мембрану - погружена гидрофобной фитольной цепью в ее липидную часть. Чистый раствор хлорофилла а имеет максимум поглощения при 663 нм. В интактной, неповрежденной, нормально функционирующей клетке хлорофилл характеризуется еще максимумами поглощения при 672 и 683 нм. Высокая эффективность поглощения света хлорофиллами обусловлена наличием в их молекуле большого числа сопряженных двойных связей.
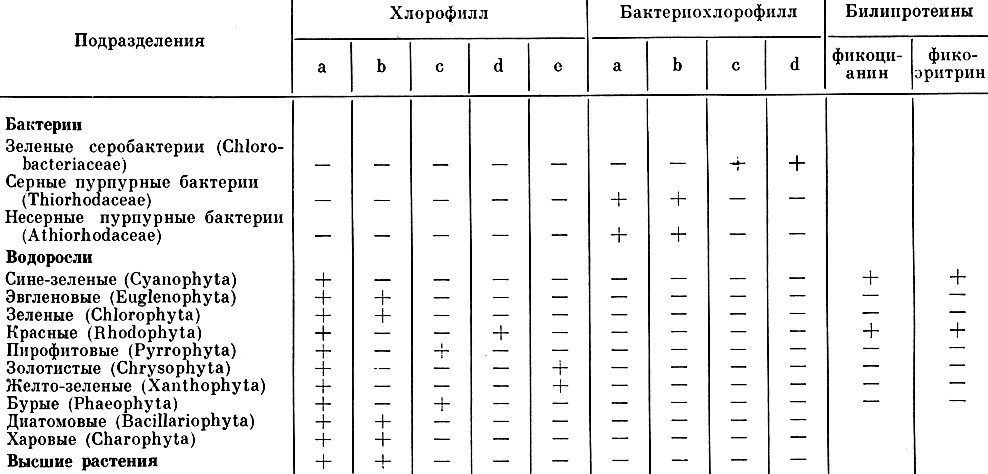
Таблица I. Распространение в растительном мире хлорофиллов и билипротеинов
Большинство выделяющих кислород фото-синтезирующих клеток содержат два разных хлорофилла, одним из которых всегда является хлорофилл а; другим же, как видно из таблицы, у разных растений являются разные хлорофиллы (b, с, d); в некоторых случаях вместо второго хлорофилла в клетке содержатся билипротеины. Дополнительными рецепторами световой энергии являются также входящие в состав фотосинтетических мембран желтые пигменты - каротиноиды. Они отличаются от хлорофилла по положению максимумов поглощения и используют непоглощаемую хлорофиллом часть видимого спектра. Предполагают также, что каротиноиды выполняют защитную функцию, предотвращая распад хлорофилла под действием молекулярного кислорода.
С помощью тонких методов спектроскопии в составе фотосинтезирующих клеток обнаружен находящийся в очень небольшом количестве пигмент с максимумом поглощения при 700 нм. Этот пигмент получил название пигмента Р700. Он отличается тем, что легко обесцвечивается под влиянием света и сильных окислителей. Полагают, что пигмент Р700 локализован в "активных центрах", представляет собой специализированную форму хлорофилла и выполняет роль "ловушки" квантов энергии, поступающих от основной массы молекул хлорофилла, функционирующих как "антенна" или своеобразный "сборщик" квантов света.
Механизм фотосинтеза
Преобразование энергии света в химическую энергию продуктов фотосинтеза представляет сложную цепь взаимосвязанных реакций, в которых участвуют многие соединения и структурные компоненты хлоропласта.
Цепь реакций, составляющих процесс фотосинтеза, можно разбить на три основные стадии:
1. Фотофизическая стадия поглощения квантов света пигментами, превращение энергии света в пигментных структурах и передача поглощенной световой энергии "активному центру".
2. Первичные фотохимические реакции, перенос электрона в электрон-транспортной цепи фотосинтеза и сопряженные с ним процессы образования "восстановительной силы".
3. Использование "восстановительной силы" для восстановления углекислоты и синтеза углеводов.
Пигменты фотосинтетического аппарата организованы в хлоропластах растений в два функциональных ансамбля, каждый из которых связан, в свою очередь, с определенной цепью переноса электронов. Эти функциональные системы получили название пигментных систем I и II (цв. табл. 1).
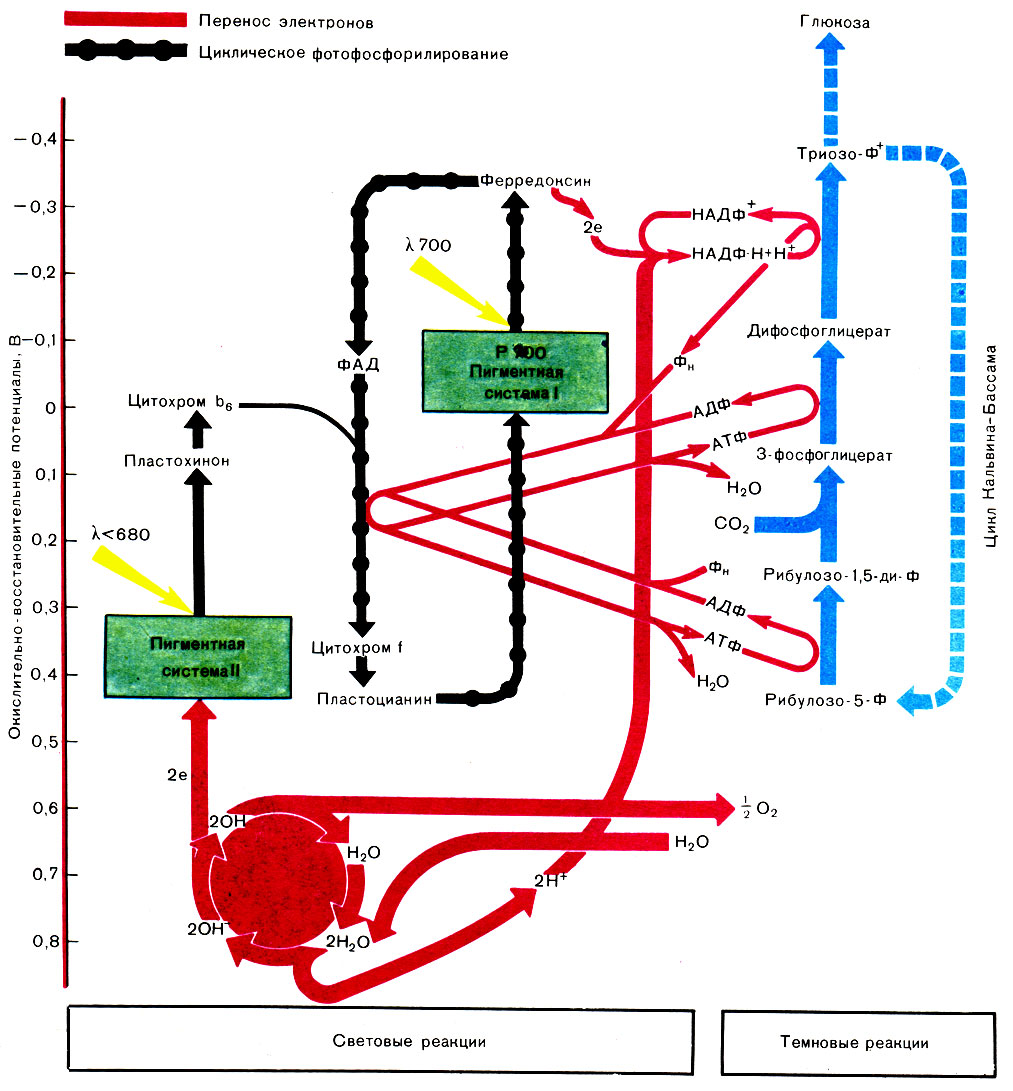
Таблица 1. Схема переноса электронов и взаимосвязи световых и темновых реакций в фотосинтезе. В состав пигментной системы I входят хлорофилл а и каротиноиды. В состав пигментной системы II входят хлорофилл а и хлорофилл b
Как подчеркивалось выше, специфическим свойством фотоавтотрофного питания зеленых растений является то, что для восстановления углекислоты в этом процессе в качестве донора водорода (электрона) используется вода и процесс идет с выделением кислорода. Это значит, что перепад окислительно-восстановительных потенциалов (ΔE0'), в пределах которого должен быть осуществлен перенос электрона, лежит между потенциалом кислородного электрода (Е0' для системы О2/Н2О при рН 7 составляет - 0,8 В) и потенциалом, который близок к водородному электроду и при котором идет восстановление пиридиннуклеотида при участии ферредоксина (Е0' для системы Н2/Н+ при рН 7 составляет +0,42 В). Таким образом, фотосинтез в интактных растениях идет в диапазоне окислительно-восстановительных потенциалов от - 0,8 до +0,42 В, т. е. около 1,2 В, что соответствует увеличению свободной энергии системы (в расчете на 1 грамм-моль) на 504 000 Дж.
Каким же образом осуществляется за счет энергии света перенос электрона в таком диапазоне окислительно-восстановительных потенциалов? Принципиальная схема этого процесса представлена на цветной таблице 1.
Процесс фотосинтеза начинается с поглощения света хлорофиллом. Молекула пигмента, поглотившая квант света, переходит в возбужденное состояние, которое длится около 10-9сек, после чего молекула возвращается к исходному уровню. При этом энергия возбуждения может быть потеряна в виде тепла или флуоресценции, или передана другим, "соседним" молекулам пигмента при достаточно близком их расположении.
В результате такой миграции в ансамбле молекул хлорофилла, расположенных в районе пигмента Р700 (реакционного центра пигментной системы I) энергия возбуждения (электрон) может быть захвачена пигментом Р700 и передана им акцептору - ферредоксину. При этом потерянный электрон (протон) восполняется у Р700 пластоцианином и снова может быть "переброшен" за счет энергии света ферредоксину.
Аналогичная картина происходит и в пигментной системе II, у которой роль акцептора электрона выполняет пластохинон, передавая полученный электрон по электрон-транспортной цепи цитохрому b, цитохрому f и, наконец, пластоцианину. Таким образом, благодаря окислительно-восстановительным превращениям промежуточных переносчиков, осуществляется постепенное движение электрона, которое индуцировано энергией кванта света.
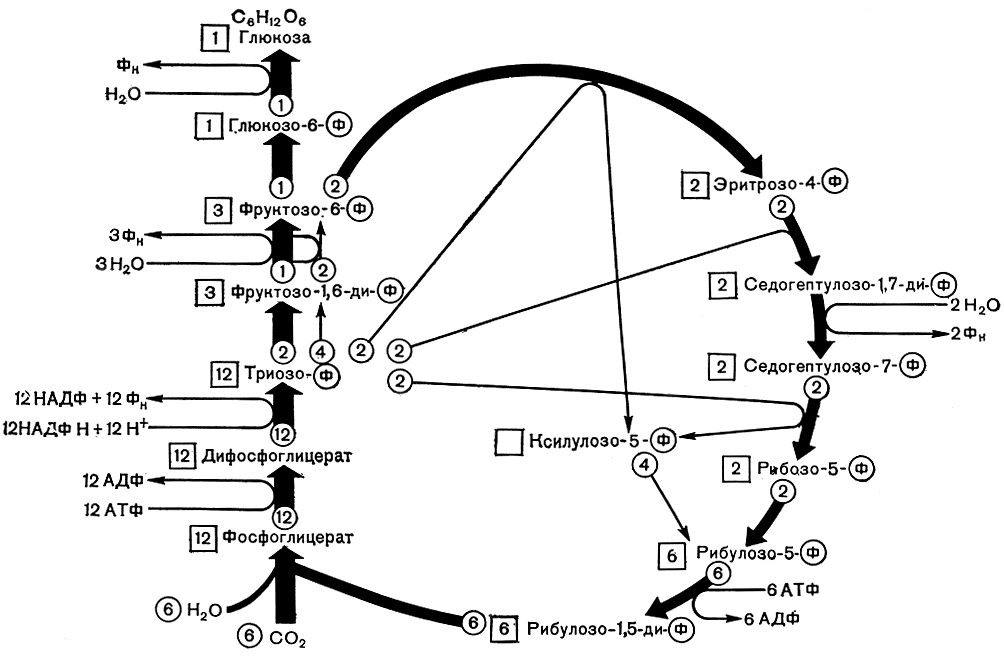
Рис. 1. Схема восстановления углерода и образования первичных продуктов фотосинтеза в растениях (пентозофосфатный восстановительный цикл углерода Кальвина). В осуществлении процесса участвуют 13 различных ферментов. Цифры, заключенные в квадрат, обозначают число молекул, образовавшихся в предыдущих реакциях. Цифры, заключенные в кружок, обозначают число молекул, используемых в различных процессах
Следует сказать, что донором электрона для пигментной системы II является в конечном итоге система фотоокисления воды, так же как и донором протона, хотя промежуточные продукты фотоокисления воды до сих пор не удалось найти и природа промежуточного донора электрона для пигментной системы II остается неизвестной. Совершенно неясным остается также механизм выделения молекулярного кислорода.
Важным обстоятельством является то, что в процессе передачи электрона в окислительно-восстановительных реакциях электрон-транспортной цепи, а именно на этапе передачи электрона от цитохрома b к цитохрому f, происходит синтез молекул аденозинтрифосфорной кислоты (АТФ) из аденозиндифосфорной кислоты (АДФ) и неорганического фосфата (Фн) в результате реакции так называемого циклического фотофосфорилирования:
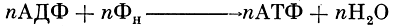
Кроме того, благодаря участию ферредоксина происходит образование АТФ и восстановленного никотинамидадениндинуклеотида (НАДФ ⋅ Н) в реакциях нециклического фотофосфорилирования:
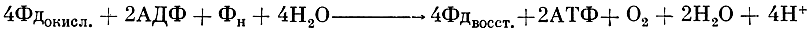
Возникающие в результате световых реакций АТФ и НАДФ⋅Н получили название восстановительной или ассимиляционной силы и используются в дальнейшем в темновых реакциях фотосинтеза для восстановления углекислоты и синтеза углеводов в пентозофосфатном цикле восстановления углерода (цикле Кальвина). Этот цикл, как видно на рисунке 1, представляет собой достаточно сложную систему ферментативных реакций, в результате которых происходят фиксация и восстановление СО2 и циклическое воспроизводство первичного акцептора углекислоты - рибулозо-1,5-дифосфата.
Последующее преобразование продуктов фотосинтеза в реакциях обмена веществ, общих для гетеротрофных и автотрофных организмов, приводит к образованию аминокислот, белков, липидов, нуклеиновых кислот и других важнейших соединений живой клетки.
Фототрофный, гетеротрофный и миксотрофный типы питания водорослей
Фотоавтотрофный способ питания с помощью фотосинтеза по масштабам и значимости стал, как мы видели, одним из основных способов питания водорослей и других зеленых растений. В разных отделах водорослей есть виды, которые являются строгими (облигатными) фотосинтетиками. К их числу относятся, например, из сине-зеленых водорослей Anabaena cylindrica, A. variabilis, Anacystis nidulans, некоторые штаммы Nostoc muscorum и др.; из зеленых - ряд видов Chlorococcum, некоторые виды Chlamydomonas, такие виды Xanthophyta, как Polyedriella helvetica и Monodus subterranea; ряд штаммов диатомей.
Однако многие водоросли обладают способностью достаточно легко переключаться в определенных условиях с фотоавтотрофного способа питания на ассимиляцию различных органических соединений и осуществлять гетеротрофный или фотогетеротрофный тип питания или сочетать эти способы питания с фотосинтезом.
Способность к росту на органических средах в темноте или на свету в отсутствие СО2 показана для большого числа видов, относящихся к сине-зеленым, зеленым, желто-зеленым, диатомовым и другим водорослям.
Известны также формы водорослей, которые относятся к числу ауксотрофных организмов и нуждаются в экзогенных источниках некоторых физиологически активных органических веществ, в частности в витаминах В12, В17 в биотине.
Таким образом, многие водоросли, обладая способностью осуществлять фотосинтез, не являются в то же время облигатными фотоавтотрофными организмами и отличаются высокой пластичностью и большим разнообразием типов питания.
Способность водорослей усваивать те или иные органические вещества существенным образом зависит не только от химической природы этих веществ, но и от генетических свойств штамма. Так, например, сравнительное изучение способности различных видов и штаммов хлореллы использовать для гетеротрофного роста (в темноте) такие углеводы, как глюкоза, галактоза, манноза, фруктоза, арабиноза, мальтоза, лактоза и сахароза, показало, что наилучшим источником углерода для большинства культур является глюкоза. Вместе с тем среди изученных форм хлореллы были обнаружены и такие штаммы, которые росли на галактозе значительно лучше, чем на глюкозе. Ряд штаммов эффективно использовали как глюкозу, так и галактозу. Некоторые формы использовали фруктозу примерно так же, как глюкозу, но в несколько раз хуже росли на среде с галактозой. Малопригодными в качестве источника углерода для большинства культур оказались манноза, фруктоза, лактоза и сахароза, хотя некоторые штаммы хлореллы могли использовать и эти сахара. Такое же разнообразие свойств штаммов в отношении их способности использовать различные сахара найдено и для других зеленых, а также сине-зеленых и желто-зеленых и некоторых других водорослей.
В качестве органического источника углерода для гетеротрофного роста водорослей пригодны также ацетат, пируват и некоторые другие органические кислоты, хотя степень и характер их использования, так же как и в случае ассимиляции Сахаров, зависит от свойств культур.
Гетеротрофный рост водорослей в темноте идет значительно медленнее, чем автотрофный рост на свету. При освещении водорослей, культивируемых на средах, например с глюкозой, но без СО2, наблюдается повышение скорости их роста и усвоения глюкозы. При этом культуры переходят к фотогетеротрофному типу питания, когда АТФ, возникающая в реакциях фотосинтетического фосфорилирования, используется для ассимиляции глюкозы. На примере ряда штаммов хлореллы показано, что в случае обеспечения углекислотой культур, выращиваемых на свету на среде с глюкозой, клетки водорослей могут переходить к миксотрофному типу питания. Скорость роста и продуктивность таких культур превышают скорость их роста при автотрофном питании и равна примерно сумме их продуктивности при фотогетеротрофном и автотрофном питании. Вместе с тем это, очевидно, не является общей закономерностью, и соотношение различных типов питания в клетках водорослей может существенно меняться в зависимости от физиолого-биохимических свойств культуры и особенностей организации внутриклеточных регуляторных процессов. В результате изучения путей биохимических превращений органических веществ, поглощаемых клетками разных водорослей в условиях фотогетеротрофного и миксотрофного питания, а также изменения активности хлоропластных и цитоплазматических ферментов при переходе от автотрофного к указанным типам питания, сейчас начинают проясняться некоторые внутренние механизмы перестройки метаболизма водорослей при смене типов питания. В ряде случаев переход к фотогетеротрофному питанию сопряжен с индукцией дополнительных ферментных систем, участвующих в преобразовании поглощаемых клеткой органических веществ. Так, например, показана индукция изоцитратлиазы у Euglena gracilis под влиянием ацетата. У некоторых форм хлореллы найдена под влиянием сахарозы индукция инвертазы, которая расщепляет молекулу этого сахара на глюкозу и фруктозу. Активность некоторых ферментов фотосинтетического аппарата, в частности ферментов цикла Кальвина, может несколько снижаться при переходе культур водорослей к использованию органических источников углерода. Поглощаемые клетками органические вещества иногда окисляются до СО2, которая в дальнейшем может использоваться в реакциях фотосинтеза. С другой стороны, может иметь место и прямое использование органических источников углерода: ацетата - через цикл глиоксиловой кислоты, глюкозы - через гексокиназную реакцию. Возможность прямой (не опосредованной через фотосинтез) ассимиляции углерода из органических источников показана, например, для Chlamydomonas mundata и Chlamydobotrys stellata, когда усвоение ацетата этими водорослями практически не изменялось при экспериментальном выключении фотосинтетического аппарата с помощью специфических ингибиторов фотосинтеза. Аналогичную картину наблюдали на Chlamydomonas reinhardii: фотосинтетический аппарат ингибировали с помощью рифампицина - специфического ингибитора синтеза хлоропластных РНК, а рост водорослей поддерживали с помощью глюкозы.
Помимо использования органических соединений в качестве источника углерода, водоросли способны переключаться с ассимиляции неорганического нитратного азота на усвоение органических источников азота - мочевины, амидов и некоторых аминокислот. Гетеротрофная ассимиляция азота - усвоение азота из органических соединений - неоднократно доказана для водорослей как факультативная форма азотного питания.
При этом, так же как и в случае усвоения углеводов и органических кислот, использование водорослями аминокислот существенным образом зависит от физиолого-биохимических свойств штаммов. Показано, что такие аминокислоты, как аргинин, гликокол, орнитин, могут использовать все штаммы хлореллы, в то время как аланин, аспарагин, серии, цистеин - только отдельные культуры. Лизин, валин, гистидин, метионин и триптофан приводили к подавлению роста некоторых форм водорослей.
Одной из характерных особенностей некоторых представителей сине-зеленых водорослей является их способность обходиться вообще без связанных форм азота и осуществлять фиксацию свободного азота атмосферы аналогично азотфиксирующим микроорганизмам.
Многообразие и пластичность способов питания водорослей позволяют им иметь широкие ареалы и занимать разнообразные экологические ниши.
Исследование способов питания водорослей позволило ввести многие из них в промышленную (массовую) культуру.
|
|
© PLANTLIFE.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://plantlife.ru/ 'PlantLife.ru: Статьи и книги о растениях'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://plantlife.ru/ 'PlantLife.ru: Статьи и книги о растениях'