
Поступление воды в вакуоль под действием осмотических сил
Поскольку большая часть присутствующей в клетке воды находится в вакуоли, мы начнем анализ проблемы транспорта воды с рассмотрения того пути, который молекуле воды требуется преодолеть для того, чтобы попасть в вакуоль клетки. Вода должна пройти сквозь две мембраны (плазмалемму и тонопласт) и через лежащую между ними цитоплазму. Мы мало знаем о различиях в способности этих трех структур пропускать воду, а потому обычно все три структуры рассматриваются совместно как единый мембранный барьер.
Для того чтобы понять, каким образом вода проходит через мембрану, представим себе, что клетка, в вакуоли которой содержатся соли, сахара, аминокислоты и прочие вещества, помещена в сосуд с дистиллированной водой (рис. 6.1). Согласно молекулярно-кинетической теории молекулы всех веществ находятся в состоянии быстрого хаотического движения, скорость которого зависит от энергии этих молекул Средняя скорость их движения определяется температурой (и служит, в сущности, ее мерой). Поскольку молекулы воды малы и проходят через клеточные мембраны намного быстрее, чем молекулы других веществ, мы можем простоты ради ограничиться рассмотрением перемещения только молекул воды. Молекулы эти диффундируют во всех направлениях: в клетку и из клетки, в различные клеточные органеллы и из них. Мы знаем, однако, что вакуоль содержит значительные количества различных растворенных веществ. Молекулы этих растворенных веществ ослабляют связи между молекулами содержащейся в вакуоли воды, притягивая их к себе и тем самым уменьшая суммарный поток воды из клетки наружу. В известном смысле растворенные вещества снижают активность молекул воды, находящихся в клетке. Как следствие этого кинетическая энергия воды в вакуоли ниже, чем относительно более чистой воды вне клетки. Сказанное означает, что снаружи вакуоли о любой участок ее мембраны ударяется в единицу времени больше молекул воды и большее их число проникает на этом участке внутрь, нежели выходит из нее. В результате этой быстрой неравномерной двусторонней диффузии молекул воды через мембрану вакуоли объем вакуоли увеличивается и создается тургор - содержимое клетки прижимается к ее стенке.
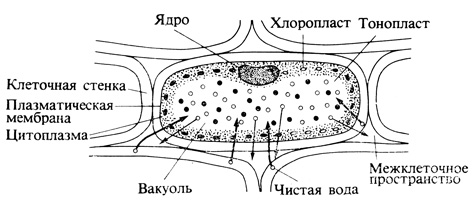
Рис. 6.1. Внутреннее давление, т. е. давление на клеточную стенку, возникает вследствие различия в скоростях перемещения воды в клетку и из клетки. Содержащиеся в вакуоли молекулы растворенных веществ (черные кружки) снижают активность молекул воды, в результате чего диффузия изнутри наружу происходит с меньшей скоростью, чем диффузия снаружи внутрь
Диффузия воды через полупроницаемую мембрану называется осмосом; концентрация растворенных веществ в вакуоли служит мерой максимальной способности клетки поглощать воду. Энергетический уровень молекул данного вещества, отражаемый скоростью их диффузии, называют химическим потенциалом этого вещества. Здесь, однако, мы говорим только о воде и потому будем пользоваться специальным, предназначенным именно для этого частного случая термином: водный потенциал. Водный потенциал (ψ) характеризует способность воды диффундировать, испаряться или поглощаться. Он имеет размерность энергии, деленной на объем (что совпадает с размерностью давления), и его величину выражают обычно в атмосферах или барах (1 бар = 0,987 атм). В действительности мы не можем измерить энергию молекул воды, например, в лабораторном стакане, поэтому условно за нуль принят ψ чистой воды при нормальных условиях (стандартных температуре и давлении). Измерить возможно только разность энергий молекул воды, находящихся в разных условиях. Чем ниже энергия молекул воды, тем ниже и водный потенциал; поскольку ψ чистой воды принят равным нулю, с увеличением концентрации растворенных веществ ψ становится все более отрицательным. При осмосе молекулы растворенного вещества снижают энергию молекул воды, так что раствор имеет более отрицательный потенциал, чем чистая вода.
Молекулы воды перемещаются всегда в направлении от более высокого водного потенциала к более низкому, подобно тому как вода течет вниз, переходя на все более низкий энергетический уровень. На водный потенциал раствора влияют помимо растворенных веществ и другие факторы, например давление; поэтому ту компоненту водного потенциала, которая определяется присутствием растворенного вещества, обозначают особым термином - осмотический потенциал (ψπ). Осмотический потенциал раствора связан прямой зависимостью с концентрацией растворенного вещества. С увеличением этой концентрации осмотический потенциал становится все более отрицательным. Если 1 моль (т. е. число граммов вещества, равное его молекулярной массе) какого-нибудь недиссоциирующего вещества, например сахарозы, растворить в 1 л воды, т. е. приготовить моляльный раствор, то осмотический потенциал такого раствора при нормальных условиях будет равен -22,7 бар. В менее концентрированных растворах осмотические потенциалы соответственно менее отрицательны.
В том случае, когда раствор отделен от чистой воды полупроницаемой мембраной, вода поступает в раствор и вследствие этого возникает давление (осмотическое давление), равное по величине, но противоположное по знаку исходному осмотическому потенциалу. Раствор обладает потенциалом, за счет которого возникает такое давление, и его можно обнаружить, если, например, этот раствор поместить в прибор, называемый осмометром (рис. 6.2). Численно осмотический потенциал равен тому давлению, которое необходимо приложить к раствору в осмометре для того, чтобы предотвратить поступление в него воды.
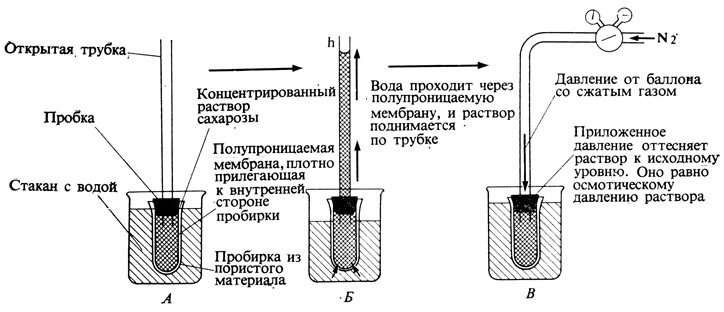
Рис. 6.2. Давление, создаваемое осмотическим движением воды, можно продемонстрировать, наблюдая за тем, до какой высоты (h) поднимется столб раствора, если отделить раствор от чистой воды полупроницаемой мембраной, пропускающей только молекулы растворителя (А, Б). Осмотическое давление измеряют, определяя то внешнее давление, которое следует приложить, чтобы предотвратить подъем раствора в трубке (В). Осмотический потенциал раствора численно равен, но противоположен по знаку максимальному осмотическому давлению, которое данный раствор способен развить. Осмотический потенциал есть у раствора всегда, даже если этот раствор в действительности и не развивает осмотического давления
Клетка, содержащая в ограниченном клеточной стенкой пространстве окруженный мембраной раствор (т. е. вакуоль), представляет собой, в сущности говоря, осмометр. Если такую клетку погрузить в чистую воду, то в нее начнет поступать вода. В отсутствие противодавления клеточной стенки поступление воды в клетку определяется водным потенциалом клетки (ψкл), в начальный момент времени равным осмотическому потенциалу (ψπ) раствора, заполняющего вакуоль. Однако с проникновением воды в вакуоль ее объем увеличивается, вода разбавляет клеточный сок и клеточная стенка начинает испытывать давление. До каких пор будет вода поступать в вакуоль? Если бы это поступление зависело только от осмотического потенциала, то теоретически оно могло бы продолжаться до бесконечности. Однако в действительности с увеличением объема вакуоли цитоплазма прижимается к клеточной стенке и возникает тургорное давление, а вместе с ним и равное ему по величине противодавление клеточной стенки на клеточное содержимое. Под потенциалом давления (ψд) понимают обычно именно противодавление клеточной стенки, но этот термин может обозначать и тургорное давление (равное первому по величине, но противоположное ему по знаку). Когда ψд достигнет достаточно большой величины, дальнейший приток воды в вакуоль прекращается. Устанавливается динамическое равновесие, при котором суммарный поток воды равен нулю, т. е. количество воды в вакуоли не изменяется, хотя молекулы воды и продолжают быстро перемещаться через мембрану в обоих направлениях. При этом положительный потенциал давления полностью уравновешивает отрицательный осмотический потенциал и клетка перестает поглощать воду; в таком состоянии ее водный потенциал равен нулю.
В любой данный момент времени водный потенциал клетки определяется разностью между потенциалом давления и осмотическим потенциалом. Если дать клетке возможность в дистиллированной воде достичь максимального тургора, то она будет поглощать воду до тех пор, пока ψд не сравняется с ψπ, т. е. ψкл не станет равным нулю. После этого она более уже не сможет поглотить воду ни из какого раствора. Не сможет она и отнять ее от другой клетки. Если рядом окажутся две клетки с разными ψкл, то вода через клеточную стенку будет переходить из клетки с более высоким (менее отрицательным) ψкл в клетку с более низким (более отрицательным) ψкл.
Рассмотрим теперь поступление воды в вакуоль и из вакуоли растительной клетки in situ (т. е. в растении). Вакуоль и окружающий ее протопласт заключены внутри клеточной стенки, через которую вода диффундирует свободно. (Клеточная стенка в этом смысле напоминает фильтровальную бумагу, которая тоже состоит из целлюлозы.) Клеточная стенка насыщена водой до тех пор, пока влажность почвы достаточна, а транспирация не слишком интенсивна. В этих условиях ψ в области клеточной стенки выше, чем в вакуоли, и суммарный поток воды направлен внутрь, в вакуоль. Иная картина наблюдается при недостатке влаги: в такие периоды в клеточных стенках может ощущаться водный дефицит и, следовательно, гр в этой области окажется ниже, чем в вакуоли. В результате вода будет оттекать из вакуоли (суммарный поток воды направлен наружу). Клетки начинают терять тургор; вследствие снижения тургорного давления они становятся вялыми и мягкими. Если из-за очень большой потери воды тургорное давление упадет до нуля, то лист завянет совсем; дальнейшая потеря воды приведет к разрыву протопластов и к гибели клеток, хотя, как мы увидим ниже, растение может избежать резкой потери воды, быстро закрыв свои устьица в ответ на недостаток влаги. Впоследствии, если клетки остались интактными, они вновь смогут поглотить воду и восстановить свой тургор; это произойдет либо при получении растением достаточного количества воды, либо в ночное время, когда транспирация практически прекращается и испарение вполне компенсируется поглощением воды из почвы.
ψ - водный потенциал; равен нулю для чистой воды; равен нулю или отрицателен для клеток (ψкл).
ψπ - осмотический потенциал; всегда отрицателен.
ψд - потенциал давления; обычно положителен в живых клетках (т. е. в клетках, содержимое которых находится под давлением), но отрицателен в клетках ксилемы (в которых создается натяжение воды).
ψкл есть суммарный результат действия ψπ и ψд:
ψкл=ψπ+ψд.
При полном тургоре ψπ=-ψд и ψкл=0.
При начальном плазмолизе ψд=0 и ψкл=ψ
В искусственных условиях удается наблюдать и более сильное сокращение протопластов. Если мы поместим кусочек ткани в раствор более концентрированный, чем вакуолярный сок, то отток воды из клеток будет продолжаться до тех пор, пока протопласты не отделятся от клеточных стенок и не сожмутся в комок в середине клетки. Наружный раствор легко проходит через клеточную стенку, которая практически не препятствует движению воды, и заполняет пространство между клеточной стенкой и сократившимся протопластом. Клетку в таком состоянии называют плазмолизированной (рис. 6.3). Если плазмолиз не слишком сильный и не слишком длительный, то клетка, после того как ее перенесут в воду, восстанавливает свой обычный тургор. В растительных клетках, испытывающих недостаток воды в воздушной среде, плазмолиза как такового не происходит, поскольку отсутствует свободный раствор, который мог бы заполнить пространство между протопластом и клеточной стенкой; в природе чрезмерный водный дефицит, по всей вероятности, приводит к разрыву и гибели клеток.
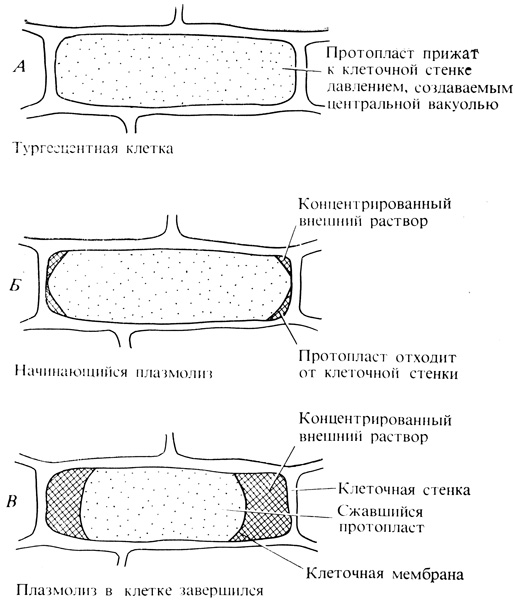
Рис. 6.3. Микрофотография, на которой виден плазмолиз в клетках чешуи луковицы. (Esau K. 1960. Plant Anatomy, 1-е изд., New York, John Willey and Sons.) Отметьте, что округлившийся протопласт отделился от клеточных стенок и переместился в середину клетки. Схема слева поясняет механизм плазмолиза
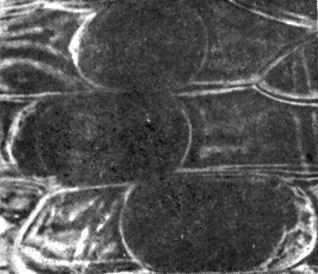
Рис. 6.3. Микрофотография, на которой виден плазмолиз в клетках чешуи луковицы. (Esau K. 1960. Plant Anatomy, 1-е изд., New York, John Willey and Sons.) Отметьте, что округлившийся протопласт отделился от клеточных стенок и переместился в середину клетки. Схема слева поясняет механизм плазмолиза
Зная ψ для данной клетки, можно предсказать, как она будет вести себя по отношению к тому или иному раствору, т. е. будет ли она поглощать воду из него или, напротив, отдавать ему воду. Для экспериментального определения ψкл отдельные клетки или кусочки ткани погружают в ряд растворов какого-нибудь вещества, например сахарозы, с постепенно возрастающей концентрацией. Водный потенциал раствора, в котором вес (или объем) клеток не увеличится и не уменьшится, и даст нам величину ψкл (рис. 6.4). Этим же методом, т. е. погружением клеток в ряд растворов с постепенно возрастающей концентрацией, можно определить и поскольку осмотический потенциал того наружного раствора, в котором начинается плазмолиз (тургор равен нулю, т. е. ψд=0), равен внутреннему осмотическому потенциалу. Начальный плазмолиз - это то состояние, при котором протопласт просто примыкает к клеточной стенке и кое-где начинает слегка от нее отставать. Поэтому определяют, просматривая под микроскопом срезы тканей, помещенные в упомянутый ряд растворов, и отмечая раствор, осмотический потенциал которого оказался как раз достаточным, чтобы вызвать плазмолиз половины клеток. Этот метод определения осмотической концентрации клеточного сока, старый и несколько примитивный, все же, по-видимому, можно считать наилучшим. В большинстве других методов требуется выжимать клеточный сок, а эта процедура, вероятно, изменяет содержимое вакуоли. Потенциал давления ψд можно измерить в крупных клетках нитчатой водоросли Nitella, вводя в них специальный микроманометр, предназначенный для таких измерений (рис. 6.5). Для высших растений измерить ψд труднее, и потому его обычно определяют как разность между ψкл и ψπ (рис. 6.4). В целых побегах клеточный водный потенциал можно измерить при помощи описанного ниже прибора.
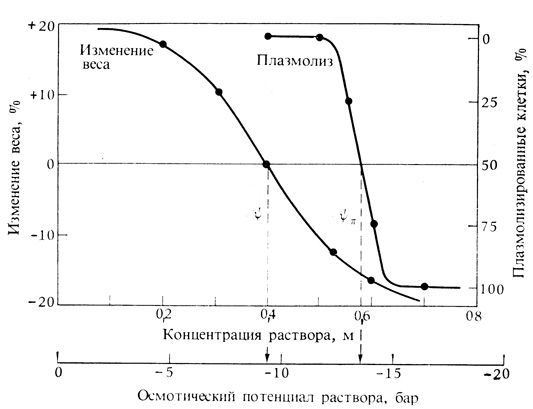
Рис. 6.4. Водный потенциал и осмотический потенциал кусочка растительной ткани (например, корня свеклы) можно измерить в лаборатории. Для того чтобы определить водный потенциал, срезы ткани помещают примерно на один час в ряд растворов сахарозы с постепенно возрастающей концентрацией. Срезы взвешивают до и после погружения в раствор. Затем строят график зависимости изменения веса от концентрации сахарозы. Водный потенциал (ψ) ткани определяется концентрацией того раствора, в котором вес среза не увеличивается и не уменьшается (т. е. раствора, с которым ткань находится в состоянии водного равновесия). Осмотический потенциал клеток растительной ткани определяют, помещая тонкие срезы ткани в ряд растворов сахарозы с постепенно возрастающей концентрацией и наблюдая при помощи микроскопа за ходом плазмолиза в этих срезах. В разбавленных растворах сахарозы плазмолиза не происходит, а в концентрированных практически все клетки оказываются плазмолизированными. Строят график зависимости между концентрацией сахарозы и процентом плазмолизированных клеток: условлено считать плазмолиз начинающимся в том растворе, где он отмечен у 50% клеток. Поскольку потенциал давления (ψд) средней клетки при начинающемся плазмолизе равен нулю, осмотический потенциал (ψπ) клеток в ткани равен ψπ того раствора, в котором плазмолизом охвачена половина клеток. Приблизительное значение потенциала давления ткани в исходном ее состоянии определится вычитанием: ψд=ψ-ψπ. Для точного определения как осмотического потенциала, так и потенциала давления следует учитывать изменение в концентрации раствора в результате оттягивания воды из плазмолизируемых клеток. В представленном здесь примере вес ткани остался неизменным в 0,4 м растворе сахарозы, а начинающийся плазмолиз наблюдался в 0,58 м растворе. Осмотический потенциал этих растворов сахарозы указан в нижней части графика. (Эти значения получены измерением в осмометре - таком, какой изображен на рис. 6.2.) Поскольку для 0,4 м раствора сахарозы ψπ=-9 бар, а для 0,58 м раствора ψπ=-13,5 бар, ψд ткани равен 4,5 бар
|
|
© PLANTLIFE.RU, 2001-2021
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://plantlife.ru/ 'PlantLife.ru: Статьи и книги о растениях'
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник:
http://plantlife.ru/ 'PlantLife.ru: Статьи и книги о растениях'